Données techniques
| Formule | C33H43N7O2 |
||||||
| Poids moléculaire | 569.74 | N° CAS | 1431612-23-5 | ||||
| Solubilité (25°C)* | In vitro | DMSO | 100 mg/mL (175.51 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In Vivo (Ajoutez les solvants au produit individuellement et dans lordre.) |
|
||||||
|
* <1 mg/ml signifie légèrement soluble ou insoluble. * Veuillez noter que Selleck teste la solubilité de tous les composés en interne, et la solubilité réelle peut différer légèrement des valeurs publiées. Ceci est normal et est dû à de légères variations dun lot à lautre. * Expédition à température ambiante (les tests de stabilité montrent que ce produit peut être expédié sans aucune mesure de refroidissement.) |
|||||||
Préparation des solutions mères
Activité biologique
| Description | UNC1999 est un inhibiteur puissant, biodisponible par voie orale et sélectif de EZH2 et EZH1 avec des IC50 de 2 nM et 45 nM dans des essais acellulaires, respectivement, montrant une sélectivité >1000 fois supérieure à un large éventail de cibles épigénétiques et non épigénétiques. Ce composé est un puissant inducteur d'autophagy. Il supprime spécifiquement H3K27me3/2 et induit une gamme d'effets anti-leucémiques, y compris l'anti-prolifération, la différenciation et l'apoptosis. | ||||
|---|---|---|---|---|---|
| Cibles |
|
||||
| In vitro | L'UNC1999 est très puissant pour les mutants EZH2 Y641N et EZH2 Y641F in vitro. Ce composé provoque des réductions concentration-dépendantes de H3K27me3 dans les cellules MCF10A avec un IC50 de 124 nM, tout en montrant une faible toxicité cellulaire. Il présente une inhibition puissante et concentration-dépendante de la prolifération cellulaire avec une EC50 de 633 nM dans une lignée cellulaire de DLBCL hébergeant le mutant EZH2Y641N. De plus, l'UNC1999 biotinylé enrichit EZH2 à partir de lysats de cellules HEK293T, et peut donc être utilisé dans des études de chimioprotéomique. | ||||
| In Vivo | Le traitement par UNC1999 (150 et 50 mg/kg, i.p.) entraîne des concentrations plasmatiques de ce composé supérieures à son IC50 cellulaire sur 24 heures in vivo. De plus, il est également biodisponible par voie orale chez la souris, ce qui rend les études animales chroniques plus pratiques et commodes. | ||||
| Caractéristiques | Le premier inhibiteur biodisponible par voie orale contre les EZH2 de type sauvage et mutant, ainsi que l'EZH1. |
Protocole (de référence)
| Test kinase : |
|
|---|---|
| Test cellulaire : |
|
| Étude animale : |
|
Références
|
Validation du produit par le client
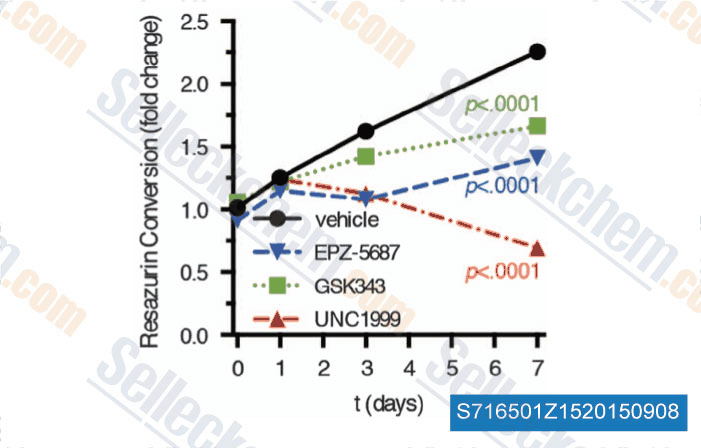
-
Données de [ , , Oncogene, 2015, 10.1038/onc.2015.38 ]
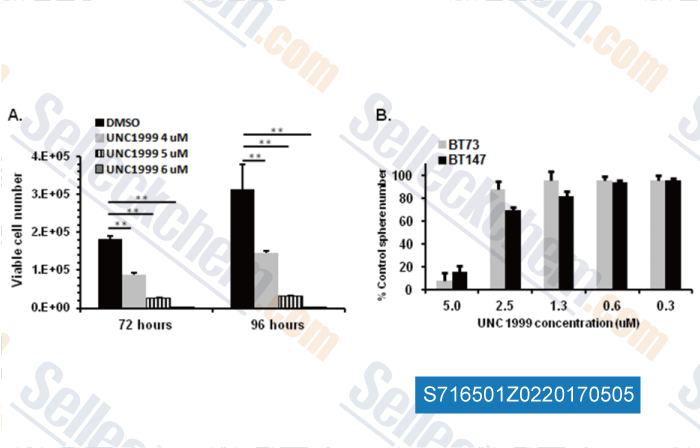
-
Données de [ , , Oncotarget, 2016, 7(37):59360-59376 ]
De Selleck UNC1999 A été cité par 34 Publications
| Inhibition of PRC2 enables self-renewal of blastoid-competent naive pluripotent stem cells from chimpanzee [ Cell Stem Cell, 2025, S1934-5909(25)00041-4] | PubMed: 40015279 |
| Chromatin modification abnormalities by CHD7 and KMT2C loss promote medulloblastoma progression [ Cell Rep, 2025, 44(5):115673] | PubMed: 40393452 |
| Epigenetic modifiers to treat retinal degenerative diseases [ bioRxiv, 2025, 2025.05.22.655558] | PubMed: 40501782 |
| LSD1 inhibition improves efficacy of adoptive T cell therapy by enhancing CD8+ T cell responsiveness [ Nat Commun, 2024, 15(1):7366] | PubMed: 39191730 |
| Ezh2 Delays Activation of Differentiation Genes During Normal Cerebellar Granule Neuron Development and in Medulloblastoma [ bioRxiv, 2024, 2024.11.21.624171] | PubMed: 39605517 |
| Hedgehog pathway orchestrates the interplay of histone modifications and tailors combination epigenetic therapies in breast cancer [ Acta Pharm Sin B, 2023, 13(6):2601-2612] | PubMed: 37425067 |
| EZH2-H3K27me3-mediated silencing of mir-139-5p inhibits cellular senescence in hepatocellular carcinoma by activating TOP2A [ J Exp Clin Cancer Res, 2023, 42(1):320] | PubMed: 38008711 |
| BRD4770 functions as a novel ferroptosis inhibitor to protect against aortic dissection [ Pharmacol Res, 2022, 177:106122] | PubMed: 35149187 |
| Dual targeting of EZH1 and EZH2 for the treatment of malignant rhabdoid tumors [ Mol Ther Oncolytics, 2022, 27:14-25] | PubMed: 36212776 |
| Enhanced Calcium Signal Induces NK Cell Degranulation but Inhibits Its Cytotoxic Activity [ J Immunol, 2022, 208(2):347-357] | PubMed: 34911773 |
POLITIQUE DE RETOUR
La politique de retour inconditionnelle de Selleck Chemical garantit une expérience dachat en ligne fluide à nos clients. Si vous nêtes en aucun cas satisfait de votre achat, vous pouvez retourner tout article dans les 7 jours suivant sa réception. En cas de problèmes de qualité du produit, quil sagisse de problèmes liés au protocole ou au produit, vous pouvez retourner tout article dans les 365 jours suivant la date dachat initiale. Veuillez suivre les instructions ci-dessous lors du retour des produits.
EXPÉDITION ET STOCKAGE
Les produits Selleck sont transportés à température ambiante. Si vous recevez le produit à température ambiante, soyez assuré que le service dinspection de la qualité de Selleck a mené des expériences pour vérifier que le placement à température normale pendant un mois naffectera pas lactivité biologique des produits en poudre. Après réception, veuillez stocker le produit conformément aux exigences décrites dans la fiche technique. La plupart des produits Selleck sont stables dans les conditions recommandées.
NON DESTINÉ À UN USAGE HUMAIN, VÉTÉRINAIRE DIAGNOSTIQUE OU THÉRAPEUTIQUE.
