uitsluitend voor onderzoeksdoeleinden
Methotrexate disodium DHFR remmer
Cat.Nr.S5097
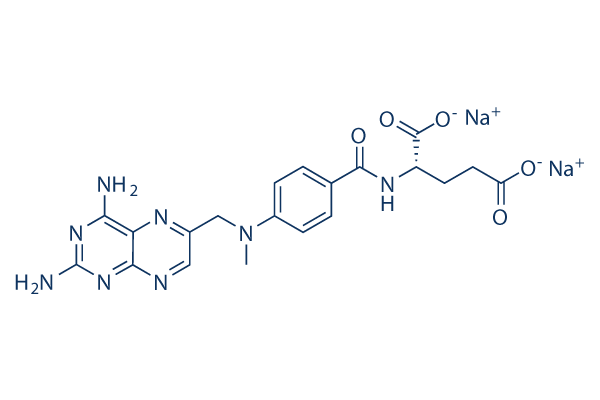
Chemische structuur
Moleculair gewicht: 498.4
Kwaliteitscontrole
| Gerelateerde doelwitten | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Overige DHFR Inhibitoren | Calcium Folinate Aminopterin Diaveridine |
Chemische informatie, Opslag en Stabiliteit
| Moleculair gewicht | 498.4 | Formule | C20H20N8O5.2Na |
Opslag (Vanaf de ontvangstdatum) | |
|---|---|---|---|---|---|
| CAS-nr. | 7413-34-5 | -- | Opslag van stamoplossingen |
|
|
| Synoniemen | Amethopterin disodium; CL14377 disodium; WR19039 disodium | Smiles | CN(CC1=CN=C2C(=N1)C(=NC(=N2)N)N)C3=CC=C(C=C3)C(=O)NC(CCC(=O)[O-])C(=O)[O-].[Na+].[Na+] | ||
Oplosbaarheid
|
In vitro |
Water : 99 mg/mL
DMSO
: Insoluble
|
Molariteitscalculator
|
In vivo |
|||||
In vivo Formuleringscalculator (Heldere oplossing)
Stap 1: Voer de onderstaande informatie in (Aanbevolen: Een extra dier voor het geval van verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in het gedeelte Oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-mastervloeistof: mg geneesmiddel vooraf opgelost in μL DMSO ( Concentratie mastervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de partij geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toeμL PEG300, mengen en helder maken, voeg vervolgens toeμL Tween 80, mengen en helder maken, voeg vervolgens toe μL ddH2O, mengen en helder maken.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toe μL Maïsolie, mengen en helder maken.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysische methoden zoals vortexen, echografie of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
hDHFR
(Activated peripheral T cells) 24 nM
|
|---|---|
| In vitro |
Methotrexate (0,1-10 mM) induceert apoptose van in vitro geactiveerde T-cellen uit humaan perifeer bloed. Methotrexate bewerkstelligt klonale deletie van geactiveerde T-cellen in gemengde lymfocytenreacties. Methotrexate kan selectief geactiveerde T-cellen uit perifeer bloed elimineren via een CD95-onafhankelijke route. Methotrexate wordt door cellen opgenomen via de gereduceerde foliumzuurdrager en wordt vervolgens binnen de cellen omgezet in polyglutamaten. Methotrexate leidt tot een verminderde productie van leukotriene B4 door ex vivo gestimuleerde neutrofielen. Methotrexate polyglutamaten remmen het enzym aminoimidazolecarboxamidoadenosineribonucleotide (AICAR) transformylase potenter dan de andere enzymen die betrokken zijn bij de purinebiosynthese. Methotrexate is ook bekend om de TNF-activiteit te onderdrukken door TNF-geïnduceerde nucleaire factor-κB-activering in vitro te onderdrukken, deels gerelateerd aan een vermindering van de afbraak en inactivatie van een remmer van deze factor, IκBα, en waarschijnlijk gerelateerd aan de afgifte van adenosine. Methotrexate onderdrukt de productie van zowel TNF als IFN-γ door T-celreceptor-geprimede T-lymfocyten van zowel gezonde menselijke donoren als RA-patiënten. Methotrexate-behandeling is geassocieerd met een significante afname van TNF-α-positieve CD4+ T-cellen, terwijl het aantal T-cellen dat het ontstekingsremmende cytokine IL-10 tot expressie brengt, toenam.
|
| In vivo |
Methotrexate verhoogt het AICAR-gehalte van splenocyten, verhoogt de adenosineconcentraties in exsudaat van carrageen-ontstoken luchtzakjes, en remt de accumulatie van leukocyten in ontstoken luchtzakjes bij muizen aanzienlijk. Methotrexate-gemedieerde reductie van leukocytenaccumulatie wordt gedeeltelijk omgekeerd door injectie van adenosine deaminase (ADA) in het luchtzakje, volledig omgekeerd door een specifieke adenosine A2-receptorantagonist, 3,7-dimethyl-1-propargylxanthine (DMPX), maar niet beïnvloed door een adenosine A1-receptorantagonist, 8-cyclopentyl-dipropylxanthine bij muizen.
|
Referenties |
|
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, kunt u een bericht achterlaten.
