기술 자료
| 화학식 | C21H22Cl2FN5O |
||||||
| 분자량 | 450.34 | CAS 번호 | 877399-52-5 | ||||
| 용해도 (25°C)* | 시험관 내(In vitro) | DMSO | 45 mg/mL (99.92 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| 생체 내(In Vivo) (개별적으로 순서대로 용매를 제품에 첨가하십시오.) |
|
||||||
|
* <1 mg/ml은 약간 용해되거나 불용해됨을 의미합니다. * Selleck은 모든 화합물의 용해도를 자체적으로 테스트하며, 실제 용해도는 게시된 값과 약간 다를 수 있습니다. 이는 정상적인 현상이며, 약간의 배치 간 변동으로 인해 발생합니다. * 실온 배송 (안정성 테스트 결과 이 제품은 냉각 조치 없이 배송될 수 있음을 보여줍니다.) |
|||||||
원액 준비
생물학적 활성
| 설명 | Crizotinib은 세포 기반 분석에서 각각 11 nM 및 24 nM의 IC50을 갖는 c-Met 및 ALK의 강력한 억제제입니다. 또한 Ki 값 0.025 nM 미만인 강력한 ROS1 억제제입니다. Crizotinib은 여러 폐암 세포주에서 STAT3 경로 억제를 통해 자가포식을 유도합니다. | ||||||
|---|---|---|---|---|---|---|---|
| 표적 |
|
||||||
| 시험관 내(In vitro) | PF-2341066은 mIMCD3 마우스 또는 MDCK 개 상피 세포에서 c-Met 인산화에 대해 유사한 효능을 보이며, IC50은 각각 5 nM 및 20 nM입니다. 이 화합물은 야생형 수용체를 발현하는 NIH3T3 세포(IC50 13 nM)와 비교하여 c-Met ATP 결합 부위 돌연변이 V1092I 또는 H1094R 또는 P-루프 돌연변이 M1250T를 발현하도록 조작된 NIH3T3 세포에 대해 IC50이 각각 19 nM, 2 nM 및 15 nM로 개선되거나 유사한 활성을 보입니다. 대조적으로, c-Met 활성화 루프 돌연변이 Y1230C 및 Y1235D를 발현하도록 조작된 세포에 대해서는 야생형 수용체와 비교하여 IC50이 각각 127 nM 및 92 nM로 이 화합물의 효능에 현저한 변화가 관찰됩니다. 또한 NCI-H69 및 HOP92 세포에서 c-Met 인산화를 강력하게 억제하며, IC50은 각각 13 nM 및 16 nM이고, 이들 세포는 내인성 c-Met 변이체 R988C 및 T1010I를 각각 발현합니다. 이 화합물은 VEGFR2 및 PDGFRβ RTK에 대해 >1,000배, IRK 및 Lck에 대해 >250배, Tie2, TrkA 및 TrkB에 대해 ~40~60배 선택성을 보이며, 모두 c-Met과 비교한 것입니다. RON 및 Axl RTK에 대해서는 20~30배 선택성을 보입니다. 대조적으로, 이 화합물은 KARPAS299 인간 역형성 대세포 림프종(ALCL) 세포주에 의해 발현되는 ALK RTK의 뉴클레오포스민(NPM)-역형성 림프종 키나제(ALK) 종양유전성 융합 변이체에 대해 거의 동일한 IC50인 24 nM을 보입니다. 암세포의 c-Met 의존성 신생물 표현형 및 내피 세포의 혈관신생 표현형을 억제합니다. 이 화학 물질은 인간 GTL-16 위암 세포 성장을 IC50 9.7 nM로 억제합니다. GTL-16 세포에서 IC50 8.4 nM로 세포자멸사를 유도합니다. HGF로 자극된 인간 NCI-H441 폐암 세포 이동 및 침윤을 IC50 11 nM 및 6.1 nM로 각각 억제합니다. MDCK 세포 산란을 IC50 16 nM로 억제합니다. HGF로 자극된 c-Met 인산화, 세포 생존 및 Matrigel 침윤을 IC50 11 nM, 14 nM 및 35 nM로 각각 억제합니다. 또한, 혈청으로 자극된 HMVEC 가지 형성 관 형성(혈관 튜브 형성)을 피브린 젤에서 억제합니다. 또한 Karpas299 또는 SU-DHL-1 ALCL 세포에서 NPM-ALK 인산화를 IC50 24 nM로 강력하게 억제합니다. 이 화합물은 세포 증식을 강력하게 억제하며, 이는 G(1)-S기 세포 주기 정지 및 ALK 양성 ALCL 세포에서 IC50 30 nM로 세포자멸사 유도와 관련이 있지만, ALK 음성 림프종 세포에서는 그렇지 않습니다. 또한, 원발성 종양 성장(즉, 증식 및 생존) 및 전이(예: 침윤 및 클론 형성)와 관련된 골육종 행동을 예방합니다. |
||||||
| 생체 내(In Vivo) | GTL-16 모델에서 PF-2341066은 50 mg/kg/일 및 75 mg/kg/일 치료 코호트 모두에서 43일 투여 일정 동안 평균 종양 부피가 60% 감소하여 크고 확립된 종양(>600 mm3)의 현저한 퇴행을 유발하는 능력을 보여줍니다. 다른 연구에서는 이 화합물이 GTL-16 종양 성장을 3개월 이상 완전히 억제하는 능력을 보였으며, 12마리 쥐 중 1마리만이 50 mg/kg/일의 3개월 치료 일정 동안 종양 성장이 유의하게 증가했습니다. NCI-H441 NSCLC 모델에서 38일 PF-2341066 투여 주기 동안 50 mg/kg/일에서 평균 종양 부피가 43% 감소하는 것이 관찰되었습니다. Caki-1 RCC 모델에서 33일 PF-2341066 투여 주기 동안 50 mg/kg/일에서 각 종양의 부피가 최소 30% 감소하는 것과 관련된 평균 종양 부피가 53% 감소하는 것이 관찰되었습니다. 이 화합물은 또한 U87MG 교모세포종 또는 PC-3 전립선암 이종이식 모델에서 50 mg/kg/일에서 확립된 종양의 성장을 거의 완전히 예방하는 것을 보여주었으며, 연구 마지막 날 각각 97% 또는 84% 억제되었습니다. 대조적으로, 50 mg/kg/일로 경구 투여된 이 화학 물질은 MDA-MB-231 유방암 모델 또는 DLD-1 결장암 모델에서 종양 성장을 유의하게 억제하지 않습니다. GTL-16 종양에서 12.5 mg/kg/일, 25 mg/kg/일 및 50 mg/kg/일에서 CD31 양성 내피 세포의 유의한 용량 의존적 감소가 관찰되었으며, 이는 MVD 억제가 항종양 효능과 용량 의존적 상관 관계를 보임을 나타냅니다. 이 화합물은 GTL-16 및 U87MG 모델 모두에서 인간 VEGFA 및 IL-8 혈장 수치의 유의한 용량 의존적 감소를 보입니다. 이 화합물의 경구 투여 후 GTL-16 종양에서 인산화된 c-Met, Akt, Erk, PLCλ1 및 STAT5 수치의 현저한 억제가 관찰되었습니다. Karpas299 ALCL 종양 이종이식을 이식한 SCID-Beige 마우스에 이 화학 물질을 경구 투여하면 초기 화합물 투여 후 15일 이내에 100 mg/kg/d 용량에서 모든 종양의 완전한 퇴행과 함께 용량 의존적 항종양 효능이 나타납니다. 또한, 포스포리파제 C-감마, 신호 전달 및 전사 활성제 3, 세포외 신호 조절 키나아제, Akt를 포함한 주요 NPM-ALK 신호 전달 매개체의 이 화합물에 의한 억제는 NPM-ALK 인산화 및 기능 억제와 상관 관계가 있는 농도 또는 용량 수준에서 관찰되었습니다. 이 화합물은 원발성 종양 성장(예: 증식 및 생존) 및 전이(예: 침윤 및 클론 형성)와 관련된 골육종 행동을 예방합니다. 이 화학 물질을 경구 위관 영양으로 처리한 누드 마우스에서 골육종 이종이식편의 성장 및 관련 골용해 및 피질외 골 기질 형성은 이 화합물에 의해 예방됩니다. 50 mg/kg의 이 화합물로 c-MET 증폭 GTL-16 이종이식편을 치료하면 18F-FDG 섭취의 느린 감소 및 포도당 수송체 1, GLUT-1의 발현 감소와 관련된 종양 퇴행이 유도됩니다. |
프로토콜 (참조)
| 키나아제 분석: |
|
|---|---|
| 세포 분석: |
|
| 동물 연구: |
|
참조
|
고객 제품 검증
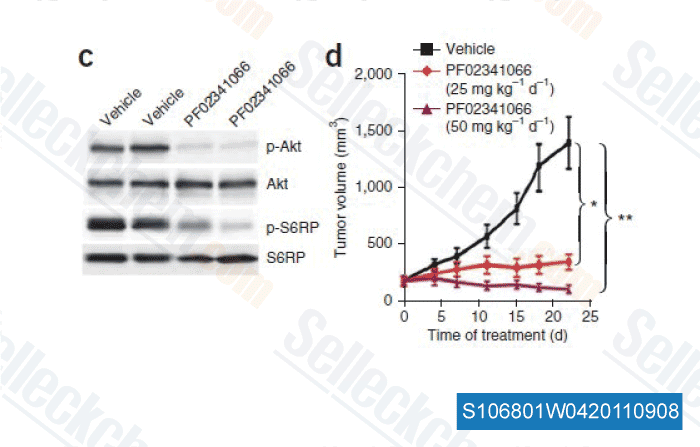
-
데이터 출처 [ Nat Med , 2011 , 17, 1116-1120 ]
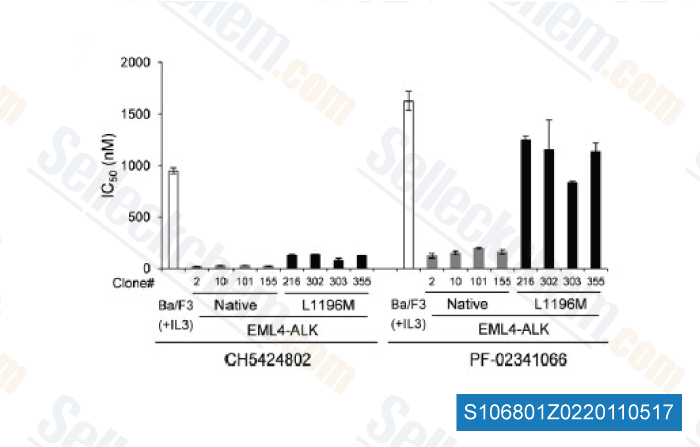
-
데이터 출처 [ Cancer Cell , 2011 , 19, 679–690 ]
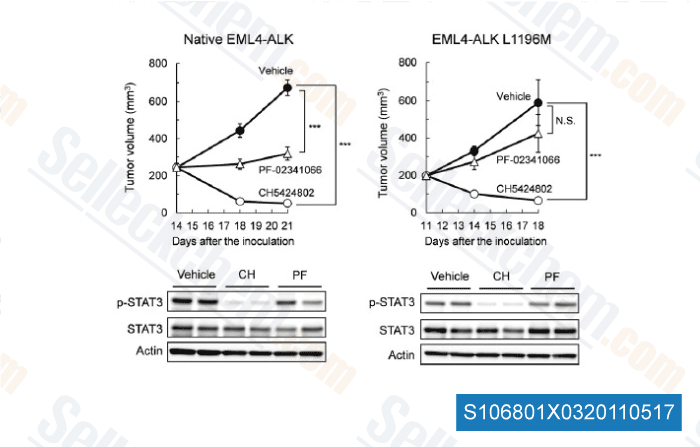
-
데이터 출처 [ Cancer Cell , 2011 , 19, 679–690 ]

-
데이터 출처 [ J Biomol Screen , 2011 , 16, 141-154 ]
Sellecks PF-02341066 (Crizotinib) 인용됨 499 출판물
| RNase1-driven ALK-activation is an oncogenic driver and therapeutic target in non-small cell lung cancer [ Signal Transduct Target Ther, 2025, 10(1):124] | PubMed: 40246819 |
| A patient-derived T cell lymphoma biorepository uncovers pathogenetic mechanisms and host-related therapeutic vulnerabilities [ Cell Rep Med, 2025, S2666-3791(25)00102-8] | PubMed: 40147445 |
| ARID1A loss enhances sensitivity to c-MET inhibition by dual targeting of GPX4 and iron homeostasis, inducing ferroptosis [ Cell Death Differ, 2025, 10.1038/s41418-025-01510-x] | PubMed: 40369167 |
| Targeting proteostasis in multiple myeloma through inhibition of LTK [ Leukemia, 2025, 10.1038/s41375-025-02682-8] | PubMed: 40634511 |
| Multi-layer stratified oncology platform utilizing transcriptomics, prostate cancer organoids, and modeling of drug response [ J Exp Clin Cancer Res, 2025, 44(1):290] | PubMed: 41094672 |
| Novel selective strategies targeting the BCL-2 family to enhance clinical efficacy in ALK-rearranged non-small cell lung cancer [ Cell Death Dis, 2025, 16(1):194] | PubMed: 40113795 |
| The Src family kinase inhibitor drug Dasatinib and glucocorticoids display synergistic activity against tongue squamous cell carcinoma and reduce MET kinase activity [ Cell Commun Signal, 2025, 23(1):293] | PubMed: 40537792 |
| MET variants with activating N-lobe mutations identified in hereditary papillary renal cell carcinomas still require ligand stimulation [ Mol Oncol, 2025, 19(8):2366-2387] | PubMed: 39980226 |
| Synergistic effects of oncogene inhibition and pyruvate dehydrogenase kinase blockade in resistant NSCLC cells [ Biochim Biophys Acta Mol Basis Dis, 2025, 1871(8):168014] | PubMed: 40784600 |
| HGF Overexpression in Mesenchymal Stromal Cell-Based Cell Sheets Enhances Autophagy-Dependent Cytoprotection and Proliferation to Guard the Epicardial Mesothelium [ Int J Mol Sci, 2025, 26(15)7298] | PubMed: 40806435 |
반품 정책
Selleck Chemical의 무조건 반품 정책은 고객에게 원활한 온라인 쇼핑 경험을 보장합니다. 구매에 어떤 식으로든 불만족하시면, 수령일로부터 7일 이내에 모든 품목을 반품하실 수 있습니다. 제품 품질 문제(프로토콜 관련 문제 또는 제품 관련 문제)가 발생하는 경우, 원래 구매일로부터 365일 이내에 모든 품목을 반품하실 수 있습니다. 제품 반품 시 아래 지침을 따르십시오.
배송 및 보관
Selleck 제품은 실온에서 운송됩니다. 실온에서 제품을 받으셨더라도 안심하십시오. Selleck 품질 검사 부서에서 한 달간의 상온 보관이 분말 제품의 생물학적 활성에 영향을 미치지 않음을 확인하는 실험을 수행했습니다. 수령 후, 데이터시트에 설명된 요구 사항에 따라 제품을 보관하십시오. 대부분의 Selleck 제품은 권장 조건에서 안정적입니다.
인간, 수의학 진단 또는 치료 용도로 사용하지 마십시오.
