réservé à la recherche
Atazanavir (BMS-232632) Sulfate HIV Protease inhibiteur
N° Cat.S1457
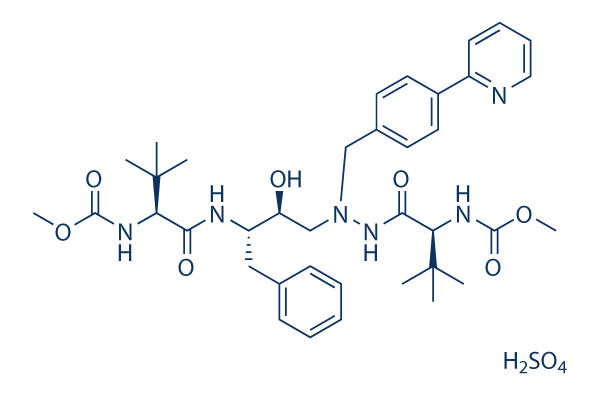
Structure chimique
Poids moléculaire: 802.93
Contrôle qualité
| Cibles apparentées | HDAC Caspase Proteasome Secretase MMP HCV Protease Cysteine Protease DPP Tyrosinase Serine Protease |
|---|---|
| Autre HIV Protease Inhibiteurs | Pepstatin A Limonin Temsavir (BMS-626529) NBD-556 Bevirimat GS-6207 Rosamultin Dextran sulfate sodium (DSS) Mericitabine Azvudine |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 802.93 | Formule | C38H52N6O7.H2SO4 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 229975-97-7 | -- | Stockage des solutions mères |
|
|
| Synonymes | BMS-232632-05, Reyataz | Smiles | CC(C)(C)C(C(=O)NC(CC1=CC=CC=C1)C(CN(CC2=CC=C(C=C2)C3=CC=CC=N3)NC(=O)C(C(C)(C)C)NC(=O)OC)O)NC(=O)OC.OS(=O)(=O)O | ||
Solubilité
|
In vitro |
DMSO
: 100 mg/mL
(124.54 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Fonctionnalités |
Atazanavir is generally more potent than other HIV-1 Prt inhibitors, including IDV, SQV, RTV, NFV, and APV.
|
|---|---|
| Targets/IC50/Ki |
HIV protease
(Cell-free assay) 2.66 nM(Ki)
|
| In vitro |
L'Atazanavir inhibe le clivage protéolytique de la polyprotéine précurseur virale gag p55 avec une IC50 d'environ 47 nM dans les cellules H9 infectées par le virus. L'Atazanavir présente une puissante activité antivirale avec une EC50 de 3.89 nM dans les souches RF/MT-2. . L'Atazanavir s'est avéré être un inhibiteur de la glucuronidation de la bilirubine avec une IC50 de 2.4 μM. L'Atazanavir inhibe l'UGT1A1 recombinante avec un Ki de 1.9 μM. L'Atazanavir inhibe la croissance cellulaire dans les lignées cellulaires de glioblastome U251, T98G et LN229, avec des niveaux de protéines GRP78 et CHOP étonnamment augmentés. L'Atazanavir provoque une augmentation proéminente des protéines polyubiquitinylées de différentes tailles dans les cellules de glioblastome U251. L'Atazanavir inhibe également le protéasome humain 20S avec une IC50 de 26 μM. L'Atazanavir (30 μM) modifie l'ampleur du stress du RE et de l'expression des gènes UPR dans les cellules HepG2. L'Atazanavir (30 mM) provoque une augmentation de 2.5 fois de l'expression de la P-gp immunoréactive avec une diminution du Rh123 intracellulaire dans les cellules LS180V. |
| Kinase Assay |
Tests de protéase
|
|
Pour déterminer les constantes d'inhibition (Ki) pour chaque inhibiteur de Prt, la Prt de type sauvage HIV-1 RF purifiée (2.5 nM) est incubée à 37 ℃ avec un substrat fluorogène de 1 μM à 15 μM dans un tampon de réaction (1 M NaCl, 1 mM EDTA, 0.1 M acétate de sodium [pH 5.5], 0.1% polyéthylène glycol 8000) en présence ou en absence d'Atazanavir. Le clivage du substrat est quantifié en mesurant une augmentation de l'émission fluorescente à 490 nM après excitation à 340 nM à l'aide d'un Cytofluor 4000. Les réactions sont effectuées en utilisant 1.36 μM, 1.66 μM, 2.1 μM, 3.0 μM, 5.0 μM ou 15 μM de substrat en présence de cinq concentrations d'Atazanavir (1.25 nM à 25 nM). Le clivage du substrat est surveillé à intervalles de 5 minutes pendant 30 minutes. Les taux de clivage sont ensuite déterminés pour chaque échantillon aux premiers points temporels de la réaction, et les valeurs de Ki sont déterminées à partir des pentes des courbes de Michaelis-Menten résultantes.
|
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
