réservé à la recherche
Quinolinic acid NMDAR agoniste
N° Cat.S3624
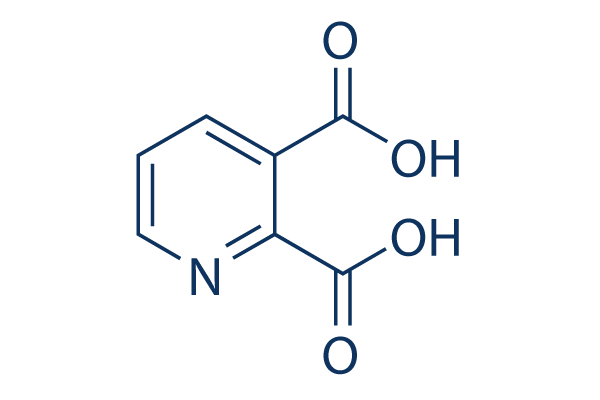
Structure chimique
Poids moléculaire: 167.12
Contrôle qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- HPLC
- SDS
- Fiche technique
Informations chimiques, stockage et stabilité
| Poids moléculaire | 167.12 | Formule | C7H5NO4 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 89-00-9 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | pyridine-2,3-dicarboxylic acid, QUIN | Smiles | C1=CC(=C(N=C1)C(=O)O)C(=O)O | ||
Solubilité
|
In vitro |
DMSO
: 25 mg/mL
(149.59 mM)
Water : 3 mg/mL Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
NMDAR
|
|---|---|
| In vitro |
La QUIN est un agoniste du récepteur N-méthyl-D-aspartate (NMDA) et possède une puissance in vivo élevée en tant qu'excitotoxine. Bien que la QUIN dispose d'un système de captage, son enzyme de dégradation neuronale est rapidement saturée, et le reste de la QUIN extracellulaire peut continuer à stimuler le récepteur NMDA. La QUIN (10 μM) prévient l'excitotoxicité induite par le glutamate dans les cultures primaires de neurones granulaires cérébelleux de rat, néanmoins, des cultures organotypiques matures du système corticostriatal ou du noyau caudé de rat chroniquement exposées à 100 nM de QUIN pendant 7 semaines maximum montrent une dégénérescence focale caractérisée par la présence de vacuoles dans le neuropile, des dendrites gonflées, des éléments postsynaptiques gonflés occasionnels et des neurones dégénérés. Le traitement in vitro de neurones fœtaux humains primaires par la QUIN entraîne une augmentation substantielle de la phosphorylation de la protéine tau à de multiples positions. L'augmentation de la phosphorylation de la protéine tau induite par la QUIN est attribuée à une diminution de l'expression et de l'activité des principales phosphatases de la protéine tau. La QUIN peut inhiber la monoamine oxydase B (MAO-B) dans les mitochondries synaptosomales du cerveau humain et peut également être un puissant inhibiteur de la phosphoénolpyruvate carboxykinase (EC 4.1.1.32) issue du cytoplasme du foie de rat, une enzyme importante de la voie de la néoglucogenèse qui convertit l'oxaloacétate en phosphoénolpyruvate. La QUIN peut augmenter la production de radicaux libres en induisant l'activité NOS dans les astrocytes et les neurones, entraînant un stress oxydatif, augmentant à la fois l'activité de la poly(ADP-ribose) polymérase (PARP) et l'activité extracellulaire de la lactate déshydrogénase (LDH).
|
| In vivo |
Quinolinic acid (QUIN), un métabolite neuroactif de la voie de la kynurénine, est normalement présent à des concentrations nanomolaires dans le cerveau humain et le liquide céphalorachidien (LCR) et est souvent impliqué dans la pathogenèse de diverses maladies neurologiques humaines. La concentration de QUIN varie selon les différentes régions du cerveau, le cortex cérébral contenant environ 1,8 nmol/g de poids humide ; presque 2 fois plus que ce que l'on trouve dans l'hippocampe (1 nmol/g de poids humide). L'administration intra-artérielle de concentrations micromolaires ou millimolaires de QUIN n'entraîne que des accumulations négligeables de ce métabolite dans le cerveau, ce qui suggère que le système nerveux central (SNC) semble être bien protégé par la barrière hémato-encéphalique (BHE) contre la QUIN périphérique. La QUIN peut également augmenter la libération de glutamate et inhiber sa recapture par les astrocytes, augmentant ainsi sa concentration dans les microenvironnements, provoquant une neurotoxicité et limitant également le recyclage du glutamate en glutamine dans les astrocytes en diminuant l'activité de la glutamine synthétase. L'injection intrastriatale de QUIN provoque une diminution de la respiration cellulaire et des niveaux d'ATP.
|
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT05513807 | Not yet recruiting | Delayed Graft Function |
Assistance Publique - Hôpitaux de Paris|Institut National de la Santé Et de la Recherche Médicale France|Centre National de la Recherche Scientifique France |
November 2022 | Phase 3 |
| NCT05718310 | Recruiting | Migraine|Migraine Disorders|Pain |
IRCCS National Neurological Institute C. Mondino Foundation|University of Pavia |
November 1 2022 | Not Applicable |
| NCT05969990 | Recruiting | Migraine in Children |
Qilu Hospital of Shandong University |
January 1 2022 | -- |
| NCT04342975 | Completed | AKI |
Mayo Clinic|Elysium Health |
December 1 2020 | Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
