réservé à la recherche
Sitagliptin DPP inhibiteur
N° Cat.S5079
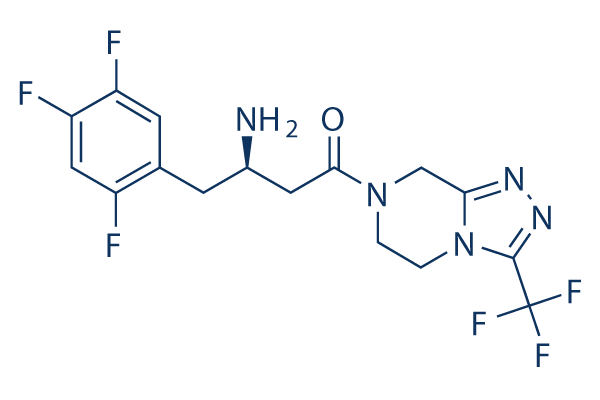
Structure chimique
Poids moléculaire: 407.31
Contrôle qualité
Informations chimiques, stockage et stabilité
| Poids moléculaire | 407.31 | Formule | C16H15F6N5O |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 486460-32-6 | -- | Stockage des solutions mères |
|
|
| Synonymes | MK-0431 | Smiles | C1CN2C(=NN=C2C(F)(F)F)CN1C(=O)CC(CC3=CC(=C(C=C3F)F)F)N | ||
Solubilité
|
In vitro |
DMSO
: 81 mg/mL
(198.86 mM)
Ethanol : 81 mg/mL Water : 5 mg/mL (Ultrasonic and heating for 10 minutes, at 60℃.) |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
DPP-4
(Cell-free) 18 nM
|
|---|---|
| In vitro |
Sitagliptin présente une marge de sélectivité > 2600 fois supérieure contre DPP8, DPP9 et d'autres membres de la famille des dipeptidyl peptidases (c'est-à-dire, la puissance contre DPP-4 vs. DPP8/9). Ce composé réduit la migration in vitro des lymphocytes T CD4 spléniques isolés via une voie impliquant l'activation de cAMP/PKA/Rac1. Il exerce une nouvelle action directe pour stimuler la sécrétion de GLP-1 par la cellule L intestinale via une voie indépendante de DPP-4, dépendante de la protéine kinase A et de MEK-ERK1/2. Il réduit donc l'effet de l'auto-immunité sur la survie des greffes.
|
| In vivo |
Sitagliptin est bien absorbé après administration orale avec une biodisponibilité de 87 %. Il a une demi-vie terminale apparente de 10 à 12 h à des doses de 25 à 100 mg et est excrété principalement (environ 80 %) sous forme inchangée par les reins. Ce composé n'interfère pas avec les enzymes du cytochrome P450 et aucune interaction médicamenteuse significative n'a été signalée. Il a été démontré qu'il inhibe l'activité de DPP-4 de > 90 % dans les 1 à 2 h suivant l'administration. Il a une courte demi-vie chez la souris (1 à 2 h). Un traitement chronique par sitagliptin dans un modèle murin non génétique de diabète de type 2 entraîne une amélioration significative du contrôle glycémique. L'amélioration de l'homéostasie du glucose est corrélée à la restauration de la masse, de l'architecture et de la capacité de sécrétion d'insuline des cellules des îlots (cellules α et β) normales en réponse à la stimulation du glucose. Ce composé prolonge la survie des greffes d'îlots chez les souris traitées par la streptozotocine et les souris NOD. L'administration de cette substance chimique in vivo réduit la migration des lymphocytes T CD4+ des ganglions lymphatiques et de la rate, mesurée in vitro, via des effets médiés par les incrétines et non médiés par les incrétines, respectivement, et les lymphocytes T CD4+ de la rate sensibles à la sDPP-IV et les lymphocytes T CD4+ des ganglions lymphatiques non sensibles aux incrétines ont sélectivement infiltré les îlots de souris NOD diabétiques, après injection dans la veine de la queue. Il a significativement supprimé l'épileptogenèse dans les crises induites par le PTZ (pentylènetétrazole). Ce composé a contrecarré les dommages neuronaux et toutes les altérations biochimiques et histo-chimiques induites par le PTZ. Le sitagliptin oral peut favoriser la neurogenèse hippocampique, contrecarrer le stress oxydatif hippocampique et prévenir le déclin des fonctions cognitives chez la souris.
|
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT05219409 | Not yet recruiting | Type 1 Diabetes |
University of Milan |
July 2023 | Phase 2|Phase 3 |
| NCT05403281 | Completed | Healthy Subjects |
Dong Wha Pharmaceutical Co. Ltd. |
November 5 2021 | Phase 1 |
| NCT03790839 | Completed | Patients |
Hua Medicine Limited |
January 31 2019 | Phase 1 |
| NCT03359590 | Completed | Pharmacological Action |
Profil Institut für Stoffwechselforschung GmbH|Merck Sharp & Dohme LLC |
March 21 2018 | Phase 2 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
