uitsluitend voor onderzoeksdoeleinden
XL147 analogue PI3K remmer
Cat.Nr.S1118
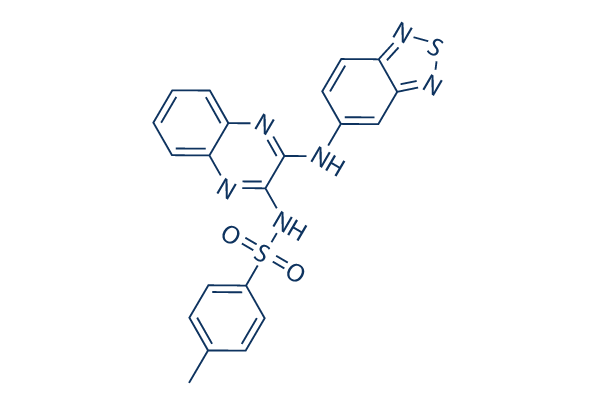
Chemische structuur
Moleculair gewicht: 448.52
Kwaliteitscontrole
| Gerelateerde doelwitten | Akt mTOR GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Overige PI3K Inhibitoren | GDC-0077 (Inavolisib) SAR405 Quercetin (Sophoretin) LY294002 Tersolisib (STX-478) Buparlisib (BKM120) 740 Y-P (PDGFR 740Y-P) GO-203 TFA Eganelisib (IPI-549) Paxalisib (GDC-0084) |
Chemische informatie, Opslag en Stabiliteit
| Moleculair gewicht | 448.52 | Formule | C21H16N6O2S2 |
Opslag (Vanaf de ontvangstdatum) | |
|---|---|---|---|---|---|
| CAS-nr. | 956958-53-5 | SDF downloaden | Opslag van stamoplossingen |
|
|
| Synoniemen | SAR245408 | Smiles | CC1=CC=C(C=C1)S(=O)(=O)NC2=NC3=CC=CC=C3N=C2NC4=CC5=NSN=C5C=C4 | ||
Oplosbaarheid
|
In vitro |
DMSO
: 3 mg/mL
(6.68 mM)
Water : Insoluble Ethanol : Insoluble |
Molariteitscalculator
|
In vivo |
|||||
In vivo Formuleringscalculator (Heldere oplossing)
Stap 1: Voer de onderstaande informatie in (Aanbevolen: Een extra dier voor het geval van verlies tijdens het experiment)
Stap 2: Voer de in vivo formulering in (Dit is alleen de calculator, geen formulering. Neem eerst contact met ons op als er geen in vivo formulering is in het gedeelte Oplosbaarheid.)
Berekeningsresultaten:
Werkconcentratie: mg/ml;
Methode voor het bereiden van DMSO-mastervloeistof: mg geneesmiddel vooraf opgelost in μL DMSO ( Concentratie mastervloeistof mg/mL, Neem eerst contact met ons op als de concentratie de DMSO-oplosbaarheid van de partij geneesmiddel overschrijdt. )
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toeμL PEG300, mengen en helder maken, voeg vervolgens toeμL Tween 80, mengen en helder maken, voeg vervolgens toe μL ddH2O, mengen en helder maken.
Methode voor het bereiden van in vivo formulering: Neem μL DMSO mastervloeistof, voeg vervolgens toe μL Maïsolie, mengen en helder maken.
Opmerking: 1. Zorg ervoor dat de vloeistof helder is voordat u het volgende oplosmiddel toevoegt.
2. Zorg ervoor dat u het/de oplosmiddel(en) in de juiste volgorde toevoegt. U moet ervoor zorgen dat de verkregen oplossing, bij de vorige toevoeging, een heldere oplossing is voordat u verdergaat met het toevoegen van het volgende oplosmiddel. Fysische methoden zoals vortexen, echografie of een warmwaterbad kunnen worden gebruikt om het oplossen te bevorderen.
Werkingsmechanisme
| Targets/IC50/Ki |
PI3Kγ
(Cell-free assay) 23 nM
PI3Kδ
(Cell-free assay) 36 nM
PI3Kα
(Cell-free assay) 39 nM
PI3Kβ
(Cell-free assay) 383 nM
|
|---|---|
| In vitro |
XL147 analogue remt klasse I PI3K-isoformen op een ATP-competitieve manier. In een panel van menselijke borstkankercellijnen die HER2 overexpressie vertonen, leidt behandeling met deze verbinding tot opheffing van AKT- en S6-fosforylering, maar induceert het ook de expressie en fosforylering van HER3 en andere RTK's. In HER2+ cellen wordt de fosforylering van HER3 gehandhaafd door de HER2-tyrosinekinase, wat leidt tot gedeeltelijk herstel van gefosforyleerd AKT (pAKT) en daardoor de antitumorale werking van deze chemische stof beperkt. Bovendien sensibiliseert knockdown van HER3 of behandeling met de anti-HER2-middelen trastuzumab of lapatinib HER2+ borstkankercellen voor dit middel in vitro en in vivo. Behandeling met deze remmer remt de monolaaggroei van alle geteste cellijnen, waaronder BT474, HCC1937 et al., op een dosisafhankelijke manier. Het belangrijkste effect van deze verbinding is remming van celproliferatie. Het induceert celdood bij een concentratie van 20 μM. Behandeling met deze chemische stof leidt tot dosisafhankelijke remming van PI3K. In overeenstemming met de remming van celproliferatie, induceert het een reductie in cycline D1 en pRB en een toename in de niveaus van de CDK-remmer p27KIPI, maar geen detecteerbare verandering in de niveaus van totale of gekliefde poly(ADP-ribose)polymerase (PARP). Behandeling met dit middel leidt tot een dosisafhankelijke reductie in pAKTS473/T308 en pS6S240/244. Verrassend genoeg veroorzaakt het ook een opregulatie van totale HER3- en/of pHER3Y1289-niveaus. In HER2-overexpresserende cellen wordt de remming van PI3K gevolgd door opregulatie van expressie en fosforylering van meerdere receptortyrosinekinasen, waaronder HER3. Knockdown van FoxO1- en FoxO3a-transcriptiefactoren voorkomt de inductie van HER3, InsR, IGF1R en FGFR2 mRNA's bij remming van PI3K. In HER2+ cellen verhoogt knockdown van HER3 met siRNA of cotreatment met de HER2-remmers trastuzumab of lapatinib de XL147-geïnduceerde celdood en remming van pAKT en pS6.
|
| In vivo |
Athymische muizen met BT474-xenografts worden willekeurig behandeld met XL147 analogue, lapatinib, trastuzumab, of deze verbinding plus elke HER2-antagonist. Elke monotherapie remt de tumorgroei significant, waarbij trastuzumab het enige middel is dat een complete tumorregressie in één van de acht muizen induceerde. Beide combinaties zijn superieur aan de respectievelijke geneesmiddelen die alleen worden gegeven. Met name de combinatie van trastuzumab en deze chemische stof, maar niet lapatinib en XL147, induceert een complete tumorrespons in drie van de acht muizen. Er is geen duidelijke geneesmiddelgerelateerde toxiciteit in een van de behandelingsarmen. De combinatie van deze verbinding plus trastuzumab voorkomt pHER3 potenter dan alle andere behandelingen. In goede overeenstemming met verschillen in tumorgroei tussen de behandelingsarmen, is nucleair pAKT lager in tumoren behandeld met XL147 plus lapatinib of deze chemische stof plus trastuzumab vergeleken met tumoren behandeld met enkelvoudige middelen. Van alle drie de enkelvoudige geneesmiddelen is deze verbinding de enige die statistisch gezien de nucleaire pAKT-niveaus onderdrukt. Er zijn geen detecteerbare veranderingen in cytoplasmatische pAKT-niveaus. Gecombineerde remming van HER2 en PI3K in HER2-afhankelijke xenografts is vereist om de signaalafgifte van de PI3K/AKT-route maximaal te remmen.
|
Referenties |
|
Informatie klinische proef
(gegevens van https://clinicaltrials.gov, bijgewerkt op 2024-05-22)
| NCT-nummer | Rekrutering | Aandoeningen | Sponsor/Medewerkers | Startdatum | Fasen |
|---|---|---|---|---|---|
| NCT01943838 | Completed | Neoplasm Malignant |
Sanofi |
October 2013 | Phase 1 |
| NCT01436565 | Completed | Solid Tumor Cancers |
Sanofi|Merrimack Pharmaceuticals |
November 2011 | Phase 1 |
| NCT01392924 | Completed | Neoplasm Malignant |
Sanofi |
August 2011 | Phase 1 |
| NCT01357330 | Completed | Solid Tumors |
Sanofi |
May 2011 | Phase 1 |
| NCT01240460 | Completed | Glioblastoma|Astrocytoma Grade IV |
Sanofi |
January 2011 | Phase 1 |
Technische ondersteuning
Tel: +1-832-582-8158 Ext:3
Als u nog andere vragen heeft, kunt u een bericht achterlaten.
