réservé à la recherche
Nuciferine 5-HT Receptor antagoniste
N° Cat.S3821
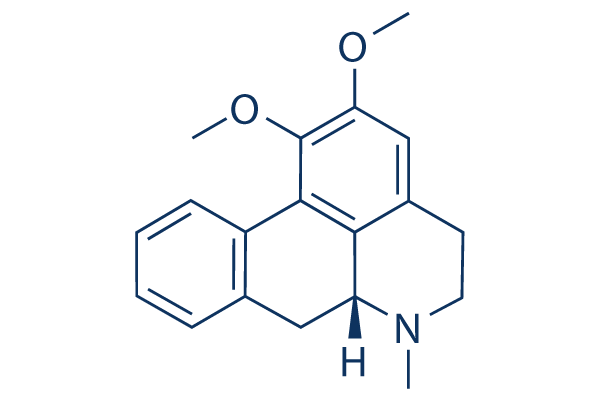
Structure chimique
Poids moléculaire: 295.38
Contrôle qualité
| Cibles apparentées | Adrenergic Receptor AChR COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Autre 5-HT Receptor Inhibiteurs | WAY-100635 Maleate Serotonin (5-HT) HCl Puerarin BRL-15572 Dihydrochloride SB269970 HCl Ketanserin RS-127445 Flopropione BRL-54443 SB742457 |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 295.38 | Formule | C19H21NO2 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 475-83-2 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | Sanjoinine E, (-)-Nuciferine, VLT 049 | Smiles | CN1CCC2=CC(=C(C3=C2C1CC4=CC=CC=C43)OC)OC | ||
Solubilité
|
In vitro |
DMSO
: 7 mg/mL
(23.69 mM)
Water : Insoluble Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| In vitro |
La Nuciferine inhibe la croissance des cellules cancéreuses du sein humaines MDA-MB-231 et MCF-7 en induisant l'apoptose et en inhibant la prolifération via l'arrêt du cycle cellulaire. Ce composé inhibe la différenciation ostéoclastique induite par le ligand du récepteur activateur du facteur nucléaire kappa-B (RANKL) dans les cellules macrophages de la moelle osseuse de souris et la résorption osseuse médiatisée par les ostéoclastes matures. Elle réduit la viabilité des cellules de neuroblastome humain SY5Y et des cellules de cancer du côlon murin CT26, et inhibe la progression du cancer du poumon non à petites cellules induite par la nicotine.
|
|---|---|
| In vivo |
Il a été constaté que la Nuciferine diminue les niveaux d'urate sérique et améliore la fonction rénale, ainsi qu'inhibe la sécrétion systémique et rénale d'interleukine-1β (IL-1β) chez les souris hyperuricémiques induites par l'oxonate de potassium. De plus, ce composé inverse l'altération de l'expression du transporteur d'urate rénal 1 (URAT1), du transporteur de glucose 9 (GLUT9), de la cassette de liaison à l'ATP, sous-famille G, membrane 2 (ABCG2), du transporteur d'anions organiques 1 (OAT1), du transporteur de cations organiques 1 (OCT1), et des transporteurs de cations organiques/carnitine 1/2 (OCTN1/2) chez les souris hyperuricémiques. Il supprime également l'activation rénale de TLR4/MyD88/NF-κB signaling et de la famille des récepteurs NOD-like, l'inflammasome NLRP3 pour réduire les niveaux sériques et rénaux d'IL-1β chez les souris hyperuricémiques avec une réduction de l'inflammation rénale.
|
Références |
|
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
