réservé à la recherche
SSR128129E FGFR inhibiteur
N° Cat.S7167
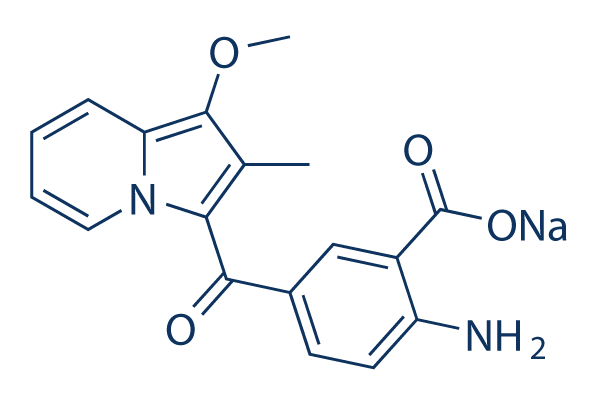
Structure chimique
Poids moléculaire: 346.31
Contrôle qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- SDS
- Fiche technique
| Cibles apparentées | EGFR VEGFR JAK PDGFR Src HIF FLT FLT3 HER2 Bcr-Abl |
|---|---|
| Autre FGFR Inhibiteurs | PD173074 AZD4547 (Fexagratinib) BLU9931 Futibatinib (TAS-120) LY2874455 PD-166866 Zoligratinib (Debio-1347) H3B-6527 Fisogatinib (BLU-554) Ferulic Acid |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 346.31 | Formule | C18H15N2O4.Na |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 848318-25-2 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | SSR | Smiles | CC1=C(N2C=CC=CC2=C1OC)C(=O)C3=CC(=C(C=C3)N)C(=O)[O-].[Na+] | ||
Solubilité
|
In vitro |
DMSO
: 69 mg/mL
(199.24 mM)
Water : 1 mg/mL Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
FGFR1
1.9 μM
|
|---|---|
| In vitro |
SSR128129E présente une activité plus efficace dans les tests cellulaires grâce à son mécanisme allostérique. Ce composé inhibe de manière dose-dépendante la prolifération et la migration des CE induites par FGF2 avec des IC50 de 31 nM et 15,2 nM, respectivement. En tant qu'inhibiteur multi-FGFR, il inhibe les réponses médiées par FGFR1-4 et entraîne ainsi le blocage de la prolifération et/ou de la migration dans diverses lignées cellulaires, y compris mPanc02, HEK-hFGFR2WT, PAE-hFGFR1, hB9-myélome et HUVEC.
|
| Kinase Assay |
Test de proximité par scintillation, liaison du 125I-FGF-2
|
|
Les billes de protéine A SPA sont fournies sous forme de suspension dans du PBS à 20 mg/mL, puis diluées avec un tampon de liaison (KCl, 400 mg/L; MgSO4 200 mg/L; NaCl 6,4 g/L; NaHCO3 3,7 g/L; NaH2PO4 0,141 mg/mL; bis Tris Propane 11,292 g/L; Glucose 4,5 g/L; Gélatine 0,1 %; pH 7,0) à 10 mg/mL. Le radioligand 125I-FGF-2 et le chimère FGFR-1IIIcß - Fc sont dilués dans le tampon de liaison. La liaison a été réalisée sur des plaques à 96 puits revêtues de 0,1 % de gélatine. Le volume total de l'essai est de 0,1 mL. La liaison du 125I-FGF-2 est déterminée par incubation des billes SPA revêtues de protéine A (0,5 mg/essai) avec le récepteur soluble chimérique FGFR-1IIIcß - Fc (5 ng/essai), le FGF-2 (20 ng/essai) est utilisé pour les déterminations de liaison non spécifique.
|
|
| In vivo |
Chez les souris atteintes d'arthrite, SSR128129E (30 mg/kg, p.o.) inhibe Angiogenesis, l'inflammation et la résorption osseuse, et réduit la gravité des symptômes cliniques. Chez les souris porteuses de divers modèles tumoraux, ce composé (30 mg/kg, p.o.) inhibe à la fois la croissance des tumeurs primaires et les métastases. De plus, il inhibe la croissance des modèles tumoraux réfractaires et sensibles à l'anti-VEGFR2, et améliore l'activité antitumorale de l'anti-VEGFR2. Ce produit chimique inhibe également l'artériosclérose dans un modèle murin de greffe veineuse et l'athérosclérose chez les souris déficientes en apolipoprotéine E.
|
Références |
|
Applications
| Méthodes | Biomarqueurs | Images | PMID |
|---|---|---|---|
| Western blot | pFGFR1 / FGFR1 / pERK / ERK / NANOG |
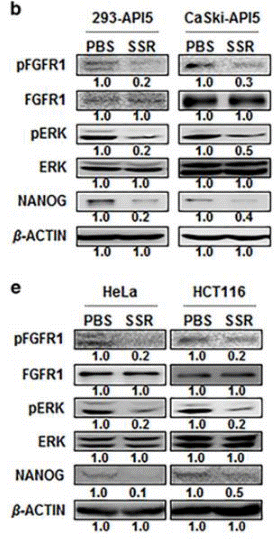
|
28092370 |
| Growth inhibition assay | Cell viability |
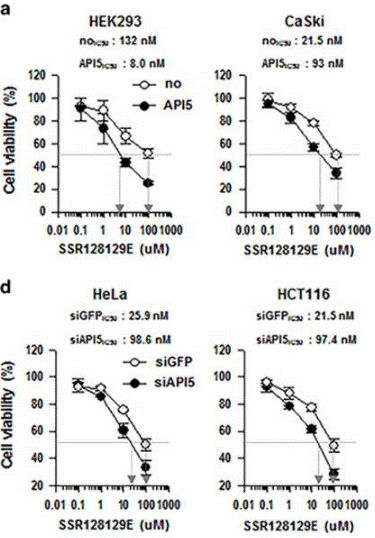
|
28092370 |
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT06194331 | Not yet recruiting | Suicidal Ideation|Suicidal and Self-injurious Behavior|Depression |
University of Pittsburgh|Pediatric Research in Office Settings|National Institute of Mental Health (NIMH) |
December 1 2024 | Not Applicable |
| NCT06175767 | Not yet recruiting | Parkinson''s Disease |
Mthera Pharma Co. Ltd. |
July 2024 | Phase 2 |
| NCT03575000 | Not yet recruiting | Schizophrenia|PreDiabetes |
VA Pittsburgh Healthcare System |
July 1 2024 | Phase 4 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
