réservé à la recherche
Ticarcillin sodium Selection Antibiotics for Transfected Cell inhibiteur
N° Cat.S3193
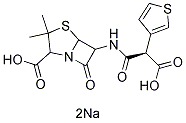
Structure chimique
Poids moléculaire: 430.41
Contrôle qualité
| Cibles apparentées | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite Reverse Transcriptase HIV |
|---|---|
| Autre Selection Antibiotics for Transfected Cell Inhibiteurs | Blasticidin S Hydrochloride Ribostamycin Sulfate D-Cycloserine |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 430.41 | Formule | C15H16N2O6S2.2Na |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 29457-07-6 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | AB 2288, BRL 2288 | Smiles | CC1(C(N2C(S1)C(C2=O)NC(=O)C(C3=CSC=C3)C(=O)[O-])C(=O)[O-])C.[Na+].[Na+] | ||
Solubilité
|
In vitro |
DMSO
: 86 mg/mL
(199.8 mM)
Water : 86 mg/mL Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| In vitro |
Les CMI de Ticarcillin (64 mg/mL) pour 90% de toutes les souches bêta-lactamase-positives sont réduites à 2 mg/mL, avec l'ajout de clavulanate. Les CMI de Ticarcillin pour 90% de toutes les souches bêta-lactamase-négatives sont de 4 mg/mL. 93,4% des souches productrices de bêta-lactamase sont sensibles au Ticarcillin à une concentration inférieure ou égale à 64 mg/mL. Ticarcillin/clavulanate de potassium est stable à la lumière et résistant à l'inactivation par la β-lactamase. Ticarcillin/clavulanate de potassium est plus économique que la carbénicilline et le céfotaxime pour éliminer Agrobacterium tumefaciens lors de la transformation végétale.
|
|---|---|
| In vivo |
La demi-vie d'élimination moyenne de Ticarcillin (120 mg/kg) dans le sérum est de 70,8 minutes chez les sujets témoins et de 53,1 minutes chez les patients atteints de mucoviscidose. La clairance corporelle totale de Ticarcillin est significativement plus élevée chez les patients atteints de mucoviscidose (65,6 mL/min/m2 contre 46,2 mL/min/m2 chez les sujets témoins). La clairance non rénale du ticarcilline est également significativement plus élevée chez les patients atteints de mucoviscidose (24,8 mL/min/m2 contre 13,3 mL/min/m2 pour le groupe témoin). Ticarcillin/clavulanate (3,1 g, administré par voie intraveineuse toutes les 4 à 6 heures) entraîne un taux de succès clinique de 80,3% et un taux d'échec clinique de 19,7% dans le traitement des infections compliquées de la peau et des structures cutanées. Le taux global d'éradication est de 83,7% dans le groupe de traitement Ticarcillin/clavulanate chez la population évaluable microbiologiquement. Ticarcillin/clavulanate entraîne des taux de guérison de 79% au moment de l'évaluation finale pour le traitement des infections intra-abdominales chez les patients pédiatriques et adultes.
|
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT01229046 | Withdrawn | Sepsis |
Phillip Brian Smith|Duke University |
September 2010 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
