réservé à la recherche
Vildagliptin DPP inhibiteur
N° Cat.S3033
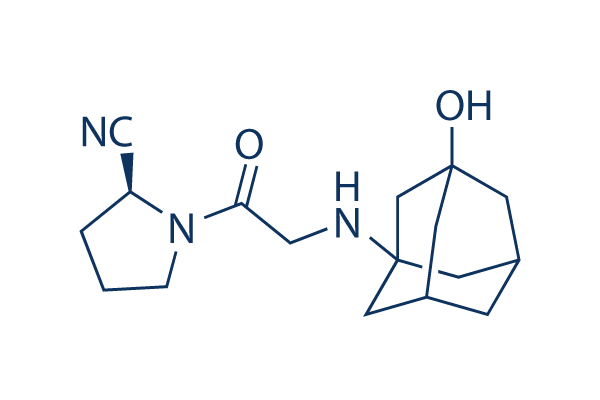
Structure chimique
Poids moléculaire: 303.4
Contrôle qualité
Culture cellulaire, traitement et concentration de travail
| Lignées cellulaires | Type dessai | Concentration | Temps dincubation | Formulation | Description de lactivité | PMID |
|---|---|---|---|---|---|---|
| Caco-2 cells | Function assay | Inhibition of human DPP4 expressed in Caco-2 cells, Ki=0.004 μM | ||||
| insect cells | Function assay | Inhibition of human recombinant His-tagged DPP4 expressed in insect cells, IC50=0.056 μM | ||||
| Cliquez pour voir plus de données expérimentales sur les lignées cellulaires | ||||||
Informations chimiques, stockage et stabilité
| Poids moléculaire | 303.4 | Formule | C17H25N3O2 |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 274901-16-5 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | LAF-237, NVP-LAF 237 | Smiles | C1CC(N(C1)C(=O)CNC23CC4CC(C2)CC(C4)(C3)O)C#N | ||
Solubilité
|
In vitro |
DMSO
: 60 mg/mL
(197.75 mM)
Water : 60 mg/mL Ethanol : 60 mg/mL |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
DPP-4
(Cell-free assay) 2.3 nM
|
|---|---|
| In vitro |
La Vildagliptine est l'inhibiteur de la DPP-IV le plus stable, se liant aux sites catalytiques S1 et S2 de la DPP-IV, possédant un mimétique de l'état de transition du site P-1. |
| In vivo |
La Vildagliptine (administrée par voie orale à raison de 10 μmol/kg) est un inhibiteur puissant et oralement actif de l'activité de la DPP-IV plasmatique qui entraîne une augmentation des niveaux de GLP-1 lors d'un test de tolérance au glucose oral (OGTT) chez des rats Zucker mâles obèses. Ce composé, administré par voie orale à raison de 10 μmol/kg, diminue significativement les excursions de glucose et stimule la sécrétion d'insuline chez les rats Zucker mâles obèses. L'inhibition maximale de l'activité de la DPP-IV plasmatique (95%) est observée environ 2 heures après l'administration de ce composé (1 μmol/kg, po) tandis qu'une inhibition >50% de la DPP-IV est observée dans les 30 min suivant l'administration et persiste pendant >10 heures chez des singes Cynomolgus normaux. Cette substance chimique (60 mg/kg) augmente la masse des cellules bêta pancréatiques grâce à une réplication accrue des cellules bêta et à une apoptose réduite, et l'augmentation de la masse des cellules bêta est maintenue pendant 12 jours après le lavage de la Vildagliptine. Ce composé administré à des doses de 10 mg/kg pendant 32 semaines protège contre la perte de fibres nerveuses chez des rats Sprague Dawley mâles adultes diabétiques induits par la streptozotocine (STZ). |
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT04081857 | Completed | Health Subjective |
Hanmi Pharmaceutical Company Limited |
June 3 2019 | Phase 1 |
| NCT04087525 | Completed | Health Subjective |
Hanmi Pharmaceutical Company Limited |
October 23 2018 | Phase 1 |
| NCT03577184 | Withdrawn | Diabetes Mellitus Type 2 |
Clinision |
July 2018 | -- |
| NCT05337969 | Completed | To Determine Bioequivalence Under Fed Conditions |
AET Laboratories Private Limited|Alfred E. Tiefenbacher (GmbH & Co. KG) |
December 2015 | Not Applicable |
| NCT05329857 | Completed | To Determine Bioequivalence Under Fed Conditions |
AET Laboratories Private Limited|Alfred E. Tiefenbacher (GmbH & Co. KG) |
December 2015 | Not Applicable |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
