réservé à la recherche
Ipragliflozin (ASP1941) SGLT inhibiteur
N° Cat.S8637
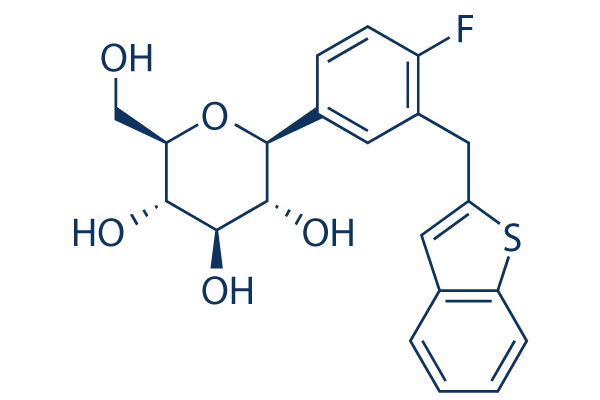
Structure chimique
Poids moléculaire: 404.45
Contrôle qualité
- Cité dans Nature Medicine pour sa qualité supérieure
- COA
- NMR
- SDS
- Fiche technique
Informations chimiques, stockage et stabilité
| Poids moléculaire | 404.45 | Formule | C21H21FOS |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 761423-87-4 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | N/A | Smiles | C1=CC=C2C(=C1)C=C(S2)CC3=C(C=CC(=C3)C4C(C(C(C(O4)CO)O)O)O)F | ||
Solubilité
|
In vitro |
DMSO
: 80 mg/mL
(197.79 mM)
Ethanol : 80 mg/mL Water : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| Targets/IC50/Ki |
mouse SGLT2
(cell-free) 5.64 nM
rat SGLT2
(cell-free) 6.73 nM
hSGLT2
(cell-free) 7.4 nM
|
|---|---|
| In vitro |
Ipragliflozin (ASP1941) inhibe l'activité du SGLT2 de souris, de rat et humain de manière concentration-dépendante à des concentrations nanomolaires. De plus, il n'inhibe pas puissamment les isoformes humaines SGLT4 et SGLT5 (IC50>1 000 nM). De plus, ce composé n'inhibe pas plusieurs isoformes du transporteur de glucose (GLUT), y compris GLUT1 et GLUT4, dans les cellules murines 3T3-L1, les cellules de rat L6, les cellules humaines Caco-2 et HepG2 (IC50>1 000 nM). Il n'interagit pas avec divers récepteurs, canaux ioniques et transporteurs tels que adrénergiques (α1, α2 et β), muscariniques (M1, M2 et non sélectif), angiotensine (AT1 et AT2), canal calcique (type L et type N), canal potassique (KATP et SKCa), canal sodique (site 2), cholécystokinine (CCKA et CCKB), dopamine (D1, D2 et transporteur), endothéline (ETA et ETB), acide gamma-aminobutyrique (GABAA et GABAB), glutamate (AMPA, kainate et NMDA), sérotonine (5-HT1, 5HT2B et transporteur), histamine (H1, H2 et H3) et neurokinine (NK1, NK2 et NK3), présentant des valeurs IC50 >3 000 nM. Il est stable contre les glucosidases intestinales de souris.
|
| In vivo |
Des doses orales uniques (0,01-10 mg/kg) d'Ipragliflozin (ASP1941) induisent une excrétion urinaire de glucose de manière dose-dépendante chez les souris normales et les souris KK-Ay, un modèle de diabète de type 2. Des administrations uniques de ce composé (0,1, 0,3 et 1 mg/kg) réduisent de manière dose-dépendante le taux de glucose sanguin chez les souris KK-Ay et les rats STZ. L'administration d'une dose unique de 0,3 mg/kg par voie intraveineuse et d'une dose unique de 1 mg/kg par voie orale à des rats révèle qu'il présente une bonne biodisponibilité avec une valeur de 71,7%. Il présente de bonnes propriétés pharmacocinétiques après administration orale et augmente de manière dose-dépendante l'excrétion urinaire de glucose, qui dure plus de 12 h chez les souris normales. Une administration unique entraîne des effets antihyperglycémiques dose-dépendants et soutenus dans les deux modèles diabétiques. Il présente un faible risque d'hypoglycémie. Après administration orale (3 mg/kg) à des souris normales, les concentrations plasmatiques atteignent un maximum à 1 h, puis diminuent progressivement. Des concentrations plasmatiques évidentes sont détectées même 8 h après l'administration. Dans les études pharmacocinétiques chez la souris, il présente une bonne biodisponibilité orale et des concentrations médicamenteuses élevées pendant de longues périodes. Les biodisponibilités absolues sont de 71,7-90,7% et 74,5-75,3% chez les rats et les singes, respectivement .
|
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT02794792 | Completed | Type 2 Diabetes Mellitus |
Astellas Pharma Europe B.V.|Astellas Pharma Inc |
May 11 2016 | Phase 3 |
| NCT02529449 | Completed | Type 1 Diabetes Mellitus |
Astellas Pharma Inc |
September 1 2015 | Phase 2 |
| NCT01972880 | Completed | Healthy|Plasma Concentration of ASP1941 |
Astellas Pharma Inc |
September 2013 | Phase 1 |
| NCT01611363 | Completed | Type 2 Diabetes Mellitus |
Astellas Pharma Europe B.V.|Astellas Pharma Inc |
October 27 2011 | Phase 1 |
| NCT01611415 | Completed | Healthy Subjects|Pharmacokinetics of Ipragliflozin |
Astellas Pharma Europe B.V.|Astellas Pharma Inc |
July 2011 | Phase 1 |
| NCT01611428 | Completed | Bioavailability of Ipragliflozin|Healthy Subjects |
Astellas Pharma Europe B.V.|Astellas Pharma Inc |
June 2011 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
