연구용
Adaptavir (DAPTA) CCR 길항제
제품 번호S8501
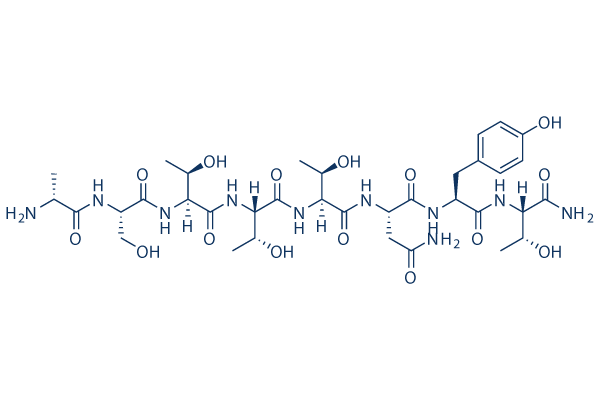
화학 구조
분자량: 856.88
품질 관리
화학 정보, 보관 및 안정성
| 분자량 | 856.88 | 화학식 | C35H56N10O15 |
보관 (수령일로부터) | |
|---|---|---|---|---|---|
| CAS 번호 | 106362-34-9 | SDF 다운로드 SDF 다운로드 | 원액 보관 |
|
|
| 동의어 | D-Ala-peptide T-amide, peptide T | Smiles | CC(C(C(=O)N)NC(=O)C(CC1=CC=C(C=C1)O)NC(=O)C(CC(=O)N)NC(=O)C(C(C)O)NC(=O)C(C(C)O)NC(=O)C(C(C)O)NC(=O)C(CO)NC(=O)C(C)N)O | ||
용해도
|
In vitro |
Water : 100 mg/mL |
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| Targets/IC50/Ki |
gp120 Bal-CCR5
(Cell-free assay) 0.06 nM
CM235-CCR5
(Cell-free assay) 0.32 nM
|
|---|---|
| 시험관 내(In vitro) |
Adaptavir (DAPTA)는 비독성 실험용 항바이러스 진입 억제제로, gp120 Bal (IC50 = 0.06 nM) 및 CM235 (IC50 = 0.32 nM)의 CCR5에 대한 특이적 CD4 의존성 결합을 강력하게 억제합니다. 공동 면역침전 연구에서 이 화합물(1 nM)은 CCR5와 gp120/sCD4 복합체 형성을 차단합니다. FITC-DAPTA가 CCR5+ 세포에는 직접 결합하지만 CCR5− 세포에는 결합하지 않는다는 공초점 현미경 연구는 CCR5가 DAPTA 수용체임을 보여줍니다. 이는 CCR5 매개 화학주성의 길항제이며, 주로 R5-영양성 HIV-1 분리주에 대해 가장 효과적인 항바이러스제로, X4-영양성 실험실 분리주에 대해서는 효과가 감소하거나 없습니다. DAPTA는 바이러스 및 세포의 높은 국소 농도를 사용하는 일반적인 분석에서 융합을 억제하지 않습니다. Th2 사이토카인 IL-4, IL-10 및 IL-13은 이 화합물에 의해 증가하며 시험관 내 감염된 대식세포에서 강력한 바이러스 정지 상태를 유도하고, 바이러스 발현을 상향 조절하는 전염증성 사이토카인 IL-1 및 TNFα의 생산을 억제합니다. 따라서 DAPTA 치료에 의한 Th2 사이토카인 증가는 대식세포 바이러스 복제를 덜 선호하게 할 것입니다.
|
| 생체 내(In vivo) |
DAPTA 치료 후, 염증성 사이토카인 IL-1, IL-6 및 TNFα 수치는 혈장에서 감소합니다. 이 화합물은 또한 gpl20과 관련된 신경 세포 사멸을 예방하고 생체 내 gpl20 관련 신경 결손을 예방합니다.
|
참조 |
|
임상시험 정보
(데이터 출처 https://clinicaltrials.gov, 업데이트 날짜 2024-05-22)
| NCT 번호 | 모집 | 조건 | 스폰서/협력자 | 시작일 | 단계 |
|---|---|---|---|---|---|
| NCT00951743 | Unknown status | HIV Infections |
Rapid Laboratories Inc. |
July 2009 | Phase 2 |
