연구용
Idarubicin HCl Topoisomerase 억제제
제품 번호S1228
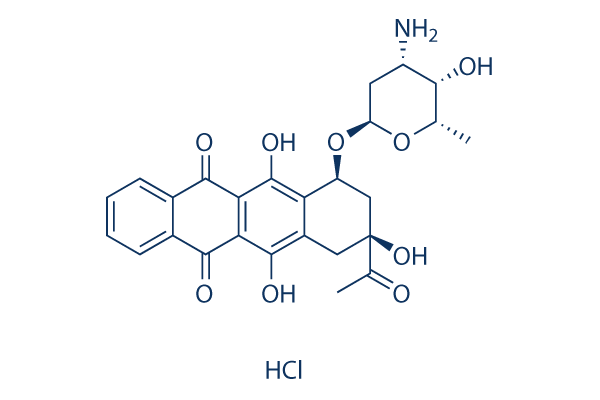
화학 구조
분자량: 533.95
품질 관리
세포 배양, 처리 및 작업 농도
| 세포주 | 분석 유형 | 농도 | 배양 시간 | 제형 | 활성 설명 | PMID |
|---|---|---|---|---|---|---|
| K562 erythroleukemic cells | Cytotoxic assay | Cytotoxic activity against K562 erythroleukemic cells, IC50=0.002 μM | 10425093 | |||
| K562 cells | Cytotoxic assay | 5 days | Cytotoxicity against human K562 cells after 5 days by XTT assay, IC50=0.012 μM | 18076140 | ||
| mouse DA-3 cells | Cytotoxic assay | 24 h | Cytotoxicity against mouse DA-3 cells after 24 hrs by XTT assay, IC50=2.3 μM | 24900668 | ||
| human ES2 cells | Cytotoxic assay | 24 h | Cytotoxicity against human ES2 cells after 24 hrs by XTT assay, IC50=3.2 μM | 24900668 | ||
| human K562 cells | Proliferation assay | 72 h | Antiproliferative activity against human K562 cells after 72 hrs, GI50=3.3 μM | 25420175 | ||
| human SKOV3 cells | Cytotoxic assay | 24 h | Cytotoxicity against human SKOV3 cells after 24 hrs by XTT assay, IC50=4.5 μM | 24900668 | ||
| HepG2 cells | Function assay | Inhibition of liver stage Plasmodium berghei infection in HepG2 cells, IC50=6.62 μM | 22586124 | |||
| human MCF7 cells | Cytotoxic assay | 24 h | Cytotoxicity against human MCF7 cells after 24 hrs by XTT assay, IC50=7.3 μM | 24900668 | ||
| mouse DA-3 cells | Cytotoxic assay | 20 μM | Cytotoxicity against mouse DA-3 cells assessed as reduction in cell viability at 20 uM by XTT assay | 24900668 | ||
| neural precursor cells | Function assay | Inhibition of neurosphere proliferation of mouse neural precursor cells by MTT assay | 17417631 | |||
| VERO-E6 | Function assay | 48 hrs | Toxicity CC50 against VERO-E6 cells determined at 48 hours by high content imaging (same conditions as 2_LEY without exposure to 0.01 MOI SARS CoV-2 virus), CC50=0.2μM | ChEMBL | ||
| 클릭하여 더 많은 세포주 실험 데이터 보기 | ||||||
화학 정보, 보관 및 안정성
| 분자량 | 533.95 | 화학식 | C26H27NO9.HCl |
보관 (수령일로부터) | |
|---|---|---|---|---|---|
| CAS 번호 | 57852-57-0 | SDF 다운로드 | 원액 보관 |
|
|
| 동의어 | 4-demethoxydaunorubicin (NSC256439, 4-DMDR) HCl | Smiles | CC1C(C(CC(O1)OC2CC(CC3=C2C(=C4C(=C3O)C(=O)C5=CC=CC=C5C4=O)O)(C(=O)C)O)N)O.Cl | ||
용해도
|
In vitro |
DMSO
: 100 mg/mL
(187.28 mM)
Water : 8 mg/mL Ethanol : Insoluble |
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| 특징 |
Idarubicin is a substrate for CYP450 2D6 and 2C9.
|
|---|---|
| Targets/IC50/Ki |
Topo II (MCF-7 cells)
(Cell-free assay) 3.3 ng/mL
Multicellular spheroids
(Cell-free assay) 7.9 ng/mL
|
| 시험관 내(In vitro) |
Idarubicin은 단층 세포에 대한 항증식 효과와 유사하게 다세포 스페로이드에 대해 유의미한 세포독성 활성을 보입니다. Idarubicin은 CYP450 2D6을 억제합니다. Idarubicin은 독소루비신과 에피루비신보다 각각 약 57.5배 및 25배 더 활성이 높습니다. Idarubicin은 P-당단백질 매개 다제내성을 극복할 수 있습니다. Idarubicin은 PMN 슈퍼옥사이드 라디칼 형성을 억제합니다. Idarubicin은 단클론 항체(anti-Ly-2.1, anti-L3T4 또는 anti-Thy-1)에 단백질 용해도 및 항체 활성 유지와 함께 결합될 수 있습니다. Idarubicin은 12 nM의 IC50으로 NALM-6 세포의 증식을 억제합니다. |
| 키나아제 분석 |
CYP450 대사 실험
|
|
CYP450 동효소 3A4, 2D6, 2C8, 2C9 및 1A2에 의한 Idarubicin 대사 평가는 각 동형에 대해 분리된 인간 CYP450 단백질을 사용하여 완료됩니다. 이러한 평가에는 고속 처리 P450 억제 테스트 방법이 활용됩니다. 대사 실험은 각 약물의 다음 특성을 조사하도록 설계되었습니다: (1) Idarubicin이 CYP450 3A4, 2C8, 2C9, 1A2 또는 2D6 동효소의 기질인지 여부; (2) 대사가 각 동효소의 알려진 억제제에 의해 영향을 받는지 여부; (3) Idarubicin이 CYP450 동효소의 억제제인지 여부; 및 (4) 카스포펑긴 또는 이트라코나졸이 Idarubicin의 CYP450 대사를 억제하는지 여부. 디벤질플루오레세인 (DBF) (CYP3A4, CYP2C8, CYP2C9), 3-시아노-7-에톡시쿠마린 (Cyp1A2) 및 7-메톡시-4-(아미노메틸)-쿠마린 (MAMC) (CYP2D6)은 각각의 동효소 활성을 확인하고 Idarubicin이 동효소 활성에 미치는 영향을 평가하는 데 사용되는 알려진 기질입니다. 또한, 케토코나졸, 쿼세틴, 설파페나졸, 푸라필린 및 퀴니딘은 각각 3A4, 2C8, 2C9, 1A2 또는 2D6 동효소에 대한 CYP450 억제제 대조군으로 사용됩니다. 지시된 대로 기질, 억제제 및 Idarubicin이 각 단백질 샘플에 첨가되고 제조업체 권장에 따라 37oC에서 20분-60분 동안 배양됩니다. 반응은 유기 용매 용액으로 중단된 다음 샘플은 적절하게 형광 플레이트 리더로 분석됩니다. 각 실험에 대해 동효소가 없는 상태에서 알려진 양의 기질 및 합성된 대사산물을 포함하는 대조군 샘플이 정성적 비교를 위해 준비됩니다. 모든 실험은 삼중으로 수행됩니다.
|
|
| 생체 내(In vivo) |
Idarubicin의 환원은 케톤 환원효소에 의존하며, 대부분의 케톤보다 더 입체선택적으로 진행되어 거의 독점적으로 (13S)-에피머를 생성합니다. Idarubicin 환원의 높은 입체특이성은 Idarubicin의 카르보닐 그룹 근처에 비대칭 중심이 존재함으로 인한 키랄 유도에서 비롯될 수 있습니다. |
참조 |
|
임상시험 정보
(데이터 출처 https://clinicaltrials.gov, 업데이트 날짜 2024-05-22)
| NCT 번호 | 모집 | 조건 | 스폰서/협력자 | 시작일 | 단계 |
|---|---|---|---|---|---|
| NCT05697510 | Recruiting | Acute Myeloid Leukemia (AML) |
Nantes University Hospital |
March 16 2023 | Phase 1 |
| NCT02652871 | Completed | Leukemia |
M.D. Anderson Cancer Center|Eli Lilly and Company|High Impact Clinical Research Support Program |
May 9 2016 | Phase 1 |
