연구용
Lumiracoxib COX 억제제
제품 번호S2903
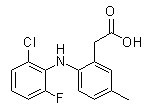
화학 구조
분자량: 293.72
품질 관리
화학 정보, 보관 및 안정성
| 분자량 | 293.72 | 화학식 | C15H13ClFNO2 |
보관 (수령일로부터) | |
|---|---|---|---|---|---|
| CAS 번호 | 220991-20-8 | SDF 다운로드 | 원액 보관 |
|
|
| 동의어 | COX-189 | Smiles | CC1=CC(=C(C=C1)NC2=C(C=CC=C2Cl)F)CC(=O)O | ||
용해도
|
In vitro |
DMSO
: 59 mg/mL
(200.87 mM)
Water : Insoluble Ethanol : Insoluble |
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| Targets/IC50/Ki |
COX-2
(Cell-free assay) 60 nM(Ki)
COX-1
(Cell-free assay) 3 μM(Ki)
|
|---|---|
| 시험관 내(In vitro) |
루미라콕시브는 COX-2를 발현하는 피부 섬유아세포에서 0.14 μm의 IC50을 가지지만, 최대 30 μm 농도(인간 COX-1으로 형질감염된 HEK 293 세포)에서는 COX-1을 억제하지 않았습니다. 인간 전혈 분석에서 이 화합물의 IC50 값은 COX-2의 경우 0.13 μM, COX-1의 경우 67 μM입니다 (COX-1/COX-2 선택성 비율 515).
|
| 생체 내(In vivo) |
Lumiracoxib는 항염증, 진통 및 해열 활성을 가진 고선택적 COX-2 억제제이며, 이는 기준 NSAID인 디클로페낙과 유사하지만 위장관 안전성이 훨씬 개선되었습니다. 이 화합물은 쥐에게 경구 투여 후 빠르게 흡수되며, 혈장 최고 농도는 0.5~1시간 사이에 도달합니다. 과통증, 부종, 발열 및 관절염 쥐 모델에서 이 화학 물질의 효능은 용량 의존적이며 디클로페낙과 유사합니다. 그러나 낮은 COX-1 억제 활성과 일치하게, 경구 100 mg/kg 용량에서는 궤양을 유발하지 않으며 디클로페낙보다 현저히 궤양 유발성이 낮습니다.
|
참조 |
임상시험 정보
(데이터 출처 https://clinicaltrials.gov, 업데이트 날짜 2024-05-22)
| NCT 번호 | 모집 | 조건 | 스폰서/협력자 | 시작일 | 단계 |
|---|---|---|---|---|---|
| NCT00350155 | Completed | Healthy Volunteers |
Novartis |
May 2006 | Phase 4 |
| NCT00348491 | Completed | Pain |
Novartis Pharmaceuticals|Novartis |
February 2006 | Phase 4 |
| NCT00267176 | Completed | Osteoarthritis|Controlled Hypertension |
Novartis Pharmaceuticals|Novartis |
November 2005 | Phase 4 |
| NCT00170872 | Completed | Osteoarthritis|Rheumatoid Arthritis |
Novartis |
November 2004 | Phase 3 |
| NCT00145301 | Completed | Osteoarthritis |
Novartis |
September 2004 | Phase 3 |
| NCT00475800 | Completed | Osteoarthritis |
Novartis |
January 2004 | Phase 3 |
