연구용
lurasidone Dopamine Receptor 길항제
제품 번호S5714
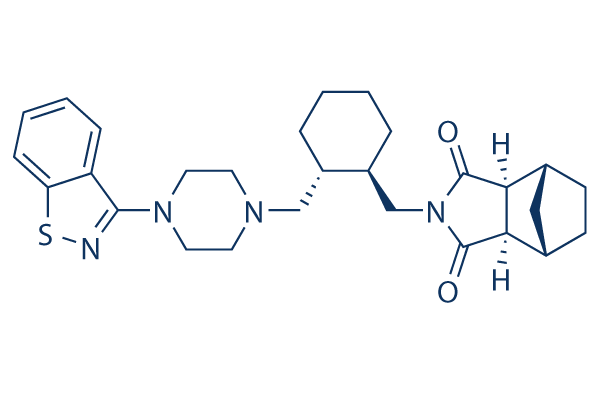
화학 구조
분자량: 492.68
품질 관리
화학 정보, 보관 및 안정성
| 분자량 | 492.68 | 화학식 | C28H36N4O2S |
보관 (수령일로부터) | 3 years -20°C powder |
|---|---|---|---|---|---|
| CAS 번호 | 367514-87-2 | -- | 원액 보관 |
|
|
| 동의어 | SM-13496 | Smiles | C1CCC(C(C1)CN2CCN(CC2)C3=NSC4=CC=CC=C43)CN5C(=O)C6C7CCC(C7)C6C5=O | ||
용해도
|
In vitro |
DMSO
: 7 mg/mL
(14.2 mM)
Water : Insoluble Ethanol : Insoluble |
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| Targets/IC50/Ki |
5-HT2A
(Cell-free assay) 0.5 nM(Ki)
5-HT7 receptor
(Cell-free assay) 0.5 nM(Ki)
D2 receptor
(Cell-free assay) 1 nM(Ki)
5-HT1A receptor
(Cell-free assay) 6.4 nM(Ki)
|
|---|---|
| 시험관 내(In vitro) |
Lurasidone은 벤조이소티아졸 계열의 새로운 비정형 항정신병 약물입니다. 대부분의 2세대 항정신병 약물과 마찬가지로 도파민 D2 및 세로토닌 5-HT2A 수용체에서 완전 길항제이며, 5-HT1A 수용체에서는 부분 효능제입니다. 다른 비정형 항정신병 약물보다 5-HT7 아형 수용체에 훨씬 더 큰 친화도를 가지고 있습니다. 이 화합물은 또한 5-HT1A 아형, 알파2c-아드레날린 수용체에 대해 높은 친화도를 가지며 알파1-아드레날린 수용체에 대해서는 낮은 친화도를 가집니다. 5-HT2C 수용체에 대한 최소한의 친화도를 가지며 히스타민 H1 및 무스카린 수용체에 대한 친화도는 무시할 만합니다.
|
| 생체 내(In vivo) |
Lurasidone은 단회 및 다회 경구 투여 후 1.5–3시간(tmax) 이내에 최고 농도에 도달하며 빠르게 흡수됩니다. 흡수된 후 조직에 광범위하게 분포하고 빠르게 중추신경계(CNS)로 들어갑니다. 이 화합물은 인간 혈장 알부민 및 알파-1-글리코프로테인에 높은 결합력을 가집니다 (>=99%). 이 약물로 조현병을 장기간 치료하면 재발 위험을 줄이는 것으로 나타났습니다. 이 화학물질의 제거 반감기는 약 20-40시간입니다. 이 약물의 평균 Cmax와 AUC(곡선 아래 면적)는 음식과 함께 투여한 경우와 공복 시 투여한 경우를 비교했을 때 각각 약 3배 및 2배 더 높았습니다. 흡수는 음식의 지방 함량과 무관합니다. 주로 CYP3A4를 통해 대사됩니다. 동물 연구에서 이 화합물은 태반 장벽을 통과하여 태아에 분포되었고, 수유 기간 동안 모유로 배설되었습니다.
|
참조 |
|
임상시험 정보
(데이터 출처 https://clinicaltrials.gov, 업데이트 날짜 2024-05-22)
| NCT 번호 | 모집 | 조건 | 스폰서/협력자 | 시작일 | 단계 |
|---|---|---|---|---|---|
| NCT03627195 | Completed | Schizophrenia |
Sumitomo Pharma America Inc. |
June 7 2018 | Phase 1 |
| NCT02731612 | Recruiting | Bipolar Disorder |
Nazlin Walji|University of British Columbia |
May 8 2017 | Phase 3 |
| NCT02147379 | Completed | Bipolar I Disorder |
University of British Columbia |
May 2014 | Phase 3 |
| NCT02174523 | Completed | Schizophrenia |
Sumitomo Pharma (Suzhou) Co. Ltd.|Xuhui Central Hospital Shanghai |
April 2014 | Phase 1 |
