연구용
Azilsartan Angiotensin Receptor 길항제
제품 번호S3046
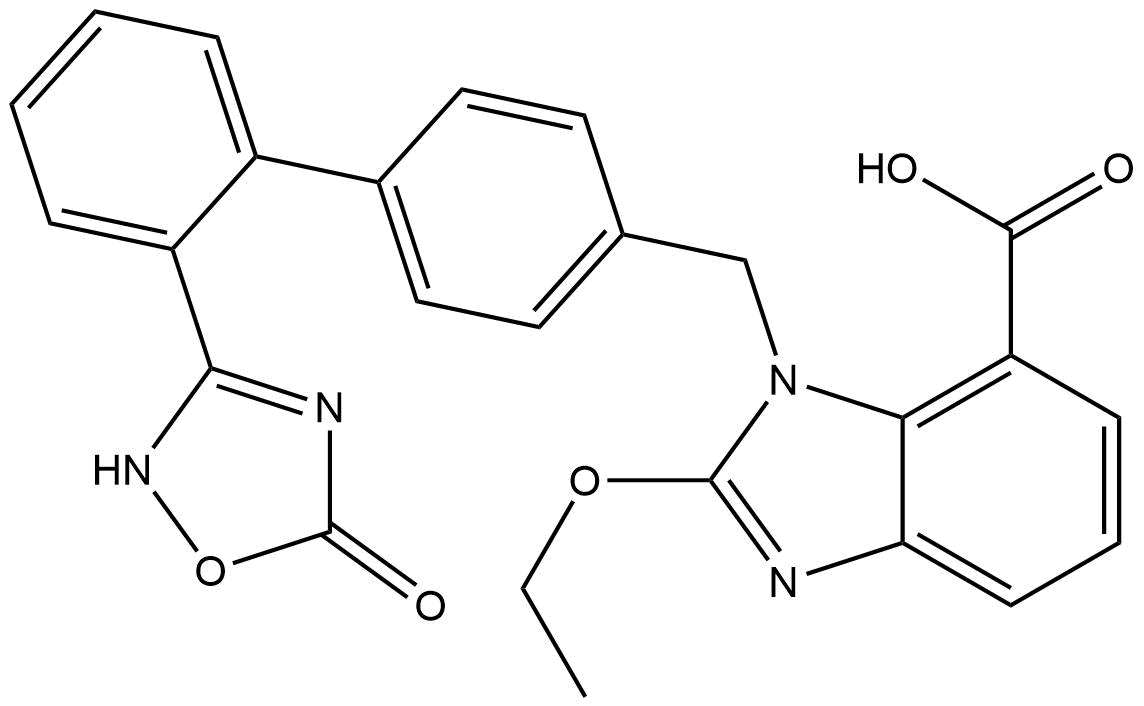
화학 구조
분자량: 456.45
품질 관리
| 관련 타겟 | CXCR Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas |
|---|---|
| 기타 Angiotensin Receptor 억제제 | PD123319 ML221 A-779 Fimasartan Olodanrigan (EMA401) Buloxibutid AVE 0991 |
화학 정보, 보관 및 안정성
| 분자량 | 456.45 | 화학식 | C25H20N4O5 |
보관 (수령일로부터) | |
|---|---|---|---|---|---|
| CAS 번호 | 147403-03-0 | SDF 다운로드 | 원액 보관 |
|
|
| 동의어 | TAK-536 | Smiles | CCOC1=NC2=CC=CC(=C2N1CC3=CC=C(C=C3)C4=CC=CC=C4C5=NOC(=O)N5)C(=O)O | ||
용해도
|
In vitro |
DMSO
: 91 mg/mL
(199.36 mM)
Water : Insoluble Ethanol : Insoluble |
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| 특징 |
A potent, orally active and specific AII receptor antagonist.
|
|---|---|
| Targets/IC50/Ki |
AT1 receptor
2.6 nM
|
| 시험관 내(In vitro) |
Azilsartan은 125I-Sar1-Ile8-AII가 인간 angiotensin type 1 수용체에 특이적으로 결합하는 것을 억제합니다. 이 화합물은 또한 세포 기반 분석에서 AII 유도 이노시톨 1-인산(IP1) 축적을 9.2 nM의 IC50 값으로 억제합니다. 분리된 토끼 대동맥 스트립에서 AII에 대한 최대 수축 반응을 pD'2 값 9.9로 감소시킵니다. AII에 의해 유도된 수축 반응에 대한 이 화학 물질의 억제 효과는 스트립을 세척한 후에도 지속됩니다. 인슐린 농도의 유의미한 변화 없이 경구 포도당 내성 검사(OGTT)에서 혈장 포도당 수치 증가를 억제하고 인슐린 감수성을 개선했습니다. 골격근에서 이 약물은 0.001% 용량으로 TNF-α 발현을 감소시킵니다. 지방 조직에서는 TNF-α 발현을 감소시키지만 아디포넥틴, PPARγ, C/EBα 및 aP2의 발현을 증가시킵니다. 배양된 3T3-L1 전지방세포에서 이 화합물은 지방 생성을 촉진하고, 발사르탄보다 퍼옥시좀 증식자 활성화 수용체-α(PPARα), PPARδ, 렙틴, 아딥신 및 아디포넥틴을 암호화하는 유전자 발현에 더 큰 영향을 미칩니다. 또한 외부에서 보충된 angiotensin II가 없는 상태에서 혈관 세포 증식을 강력하게 억제합니다.
|
| 키나아제 분석 |
인간 AT1 수용체에 대한 방사성 리간드 결합 연구
|
|
방사성 리간드 결합 분석은 4.4~6.2 fmol의 수용체/웰 (10 μg의 막 단백질/웰)을 포함하는 인간 AT1 수용체 코팅 마이크로플레이트를 사용하여 수행됩니다. 막 코팅 웰은 실온에서 다양한 농도의 Azilsartan을 포함하는 45 μL의 분석 버퍼(50 mM Tris-HCl, 5 mM MgCl2, 1 mM EDTA 및 0.005% CHAPS, pH 7.4)와 함께 배양됩니다. 90분 후, 분석 버퍼에 용해된 5 μL의 125I-Sar1-Ile8-AII (최종 농도 0.6 nM)가 웰에 첨가되고, 플레이트는 5시간 동안 배양됩니다. 각 단계에서 플레이트는 플레이트 쉐이커에서 짧고 부드럽게 흔들립니다. 세척 실험에서는 막을 이 화합물과 함께 90분 동안 배양한 다음, 결합되지 않은 화합물을 제거하기 위해 200 μL/웰의 분석 버퍼로 즉시 두 번 세척하고, 추가로 5시간 동안 125I-Sar1-Ile8-AII와 함께 배양합니다. 막 결합 방사능은 TopCount Microplate Scintillation and Luminescence Counter를 사용하여 측정됩니다. 이 화학 물질이 AT1 수용체로부터 해리 속도를 추정하기 위한 실험에서는 막을 이 화합물 30 nM 농도로 90분 동안 배양합니다. 이 화합물은 125I-Sar1-Ile8-AII가 인간 AT1에 특이적으로 결합하는 것을 약 90% 억제합니다. 막은 즉시 200 μL/웰의 분석 버퍼로 두 번 세척한 다음, 추가로 240분 동안 125I-Sar1-Ile8-AII와 함께 배양합니다. 막 결합 방사능은 TopCount Microplate Scintillation and Luminescence Counter를 사용하여 30분, 60분, 90분, 120분, 150분, 180분 또는 240분 후에 측정됩니다. 125I-Sar1-Ile8-AII의 비특이적 결합은 10 μM 비표지 AII 존재 하에서 추정됩니다. 세척 실험을 위해 세척 후 비표지 AII가 다시 첨가됩니다. 특이적 결합은 총 결합에서 비특이적 결합을 뺀 것으로 정의됩니다.
|
|
| 생체 내(In vivo) |
Koletsky 쥐에서 Azilsartan 치료는 혈압, 기저 혈장 인슐린 농도 및 인슐린 저항성 지수(HOMA-IR)를 낮추고, 경구 포도당 내성 검사 중 혈장 포도당 및 인슐린 농도의 과도한 증가를 억제했습니다. 이 화합물은 11β-hydroxysteroid dehydrogenase type 1 발현을 하향 조절합니다.
|
참조 |
|
임상시험 정보
(데이터 출처 https://clinicaltrials.gov, 업데이트 날짜 2024-05-22)
| NCT 번호 | 모집 | 조건 | 스폰서/협력자 | 시작일 | 단계 |
|---|---|---|---|---|---|
| NCT04668157 | Completed | Hypertension |
Takeda |
May 17 2021 | Phase 3 |
| NCT03434977 | Completed | Healthy Volunteers |
Takeda |
February 14 2018 | Phase 1 |
| NCT03042299 | Completed | Japanese Healthy Adult Male Participants |
Takeda |
February 10 2017 | Phase 1 |
| NCT02791438 | Completed | Pediatric Hypertension |
Takeda |
August 18 2016 | Phase 3 |
| NCT02541669 | Completed | Healthy Volunteer |
Takeda |
November 20 2015 | Phase 1 |
| NCT02451150 | Completed | Pediatric Hypertension |
Takeda |
August 2015 | Phase 3 |
