연구용
Sodium Dichloroacetate (DCA) PDK 억제제
제품 번호S8615
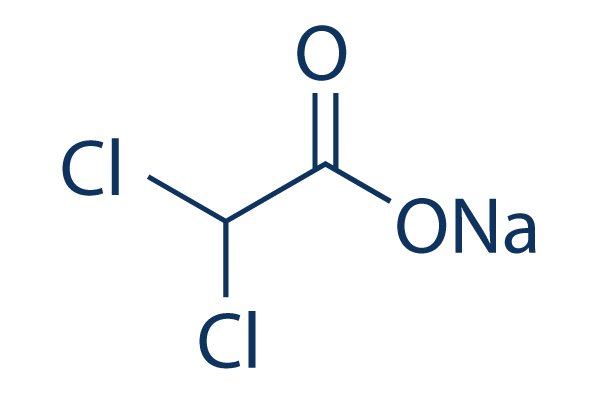
화학 구조
분자량: 150.92
품질 관리
세포 배양, 처리 및 작업 농도
| 세포주 | 분석 유형 | 농도 | 배양 시간 | 제형 | 활성 설명 | PMID |
|---|---|---|---|---|---|---|
| MCF7 | Function assay | 10 mM | 12 hrs | Inhibition of PDK1 in human MCF7 cells assessed as increase in oxygen consumption rate at 10 mM after 12 hrs | 27006991 | |
| MCF7 | Function assay | 10 mM | 12 hrs | Inhibition of PDK1 in human MCF7 cells assessed as decrease in extracellular acidification rate at 10 mM after 12 hrs | 27006991 | |
| MCF7 | Function assay | 10 mM | 12 hrs | Inhibition of PDK1 in human MCF7 cells assessed as decrease in proton production rate at 10 mM after 12 hrs | 27006991 | |
| MCF7 | Function assay | 10 mM | 12 hrs | Inhibition of PDK1 in human MCF7 cells assessed as increase in ratio of oxygen consumption rate to extracellular acidification rate at 10 mM after 12 hrs | 27006991 | |
| MCF7 | Function assay | 10 mM | 12 hrs | Inhibition of PDK1 in human MCF7 cells assessed as decrease in lactate production at 10 mM after 12 hrs | 27006991 | |
| NCI-H1975 | Antiproliferative assay | 20 mM | 72 hrs | Antiproliferative activity against human NCI-H1975 cells assessed as reduction in cell viability at 20 mM after 72 hrs by MTT assay | 30470491 | |
| MCF7 | Function assay | 90 mins | Inhibition of PDK1 (unknown origin) expressed in human MCF7 cells using PDK tide as substrate measured after 90 mins in presence of ATP by ADP-Glo luminescent kinase assay | 31509699 | ||
| MCF7 | Antitumor assay | 30 mg/kg | two weeks | Antitumor activity against human MCF7 cells xenografted in BALB/c nude mouse assessed as tumor growth inhibition at 30 mg/kg, iv administered every two days for two weeks measured after 14 days | 31509699 | |
| MCF7 | Function assay | 30 uM | 4 hrs | Induction of metabolic reversal from aerobic glycolysis to oxidative phosphorylation in human MCF7 cells assessed as increase in extracellular acidification rate at 30 uM pretreated for 4 hrs followed by glucose addition after 25 mins by seahorse XF24 ext | 31509699 | |
| MCF7 | Function assay | 30 uM | 4 hrs | Induction of metabolic reversal from aerobic glycolysis to oxidative phosphorylation in human MCF7 cells assessed as increase in extracellular acidification rate at 30 uM pretreated for 4 hrs followed by glucose addition after 25 mins followed by subsequent assay | 31509699 | |
| MCF7 | Function assay | 30 uM | 4 hrs | Induction of metabolic reversal from aerobic glycolysis to oxidative phosphorylation in human MCF7 cells assessed as decline in extracellular acidification rate at 30 uM pretreated for 4 hrs followed by glucose addition after 25 mins followed by subsequent assay | 31509699 | |
| MCF7 | Function assay | 30 uM | 6 hrs | Induction of metabolic reversal from aerobic glycolysis to oxidative phosphorylation in human MCF7 cells assessed as decrease in oxygen consumption rate at 30 uM pretreated for 6 hrs followed by oligomycin A addition after 25 mins followed by subsequent assay | 31509699 | |
| 클릭하여 더 많은 세포주 실험 데이터 보기 | ||||||
화학 정보, 보관 및 안정성
| 분자량 | 150.92 | 화학식 | C2HCl2O2.Na |
보관 (수령일로부터) | |
|---|---|---|---|---|---|
| CAS 번호 | 2156-56-1 | SDF 다운로드 | 원액 보관 |
|
|
| 동의어 | Dichloroacetic acid, bichloroacetic acid, BCA | Smiles | C(C(=O)[O-])(Cl)Cl.[Na+] | ||
용해도
|
In vitro |
|
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| Targets/IC50/Ki |
PDK4
(Cell-free assay) 80 μM
PDK2
(Cell-free assay) 183 μM
|
|---|---|
| 시험관 내(In vitro) |
Sodium Dichloroacetate (DCA)는 인간 폐암, 유방암 및 뇌암 세포의 Apoptosis를 유발할 수 있습니다. 이 화합물로 처리한 후 암세포는 시험관 내에서 ROS 수준 증가, MMP의 탈분극, 시험관 내 및 생체 내에서 Apoptosis 증가를 보입니다. 이는 피루브산 탈수소효소 키나아제 (PDK)의 활성을 억제하여 미토콘드리아 효소인 피루브산 탈수소효소 (PDH)를 자극합니다. PDH가 비활성화되면 미토콘드리아 호흡과 포도당 의존성 산화적 인산화에 필요한 피루브산을 아세틸-CoA로 더 이상 전환하지 않습니다. 따라서 DCA는 세포 Metabolism을 해당 작용에서 포도당 산화로 전환하여 미토콘드리아 막 전위 기울기를 감소시키고 미토콘드리아 전이 기공을 여는 데 도움을 줍니다. 이러한 대사 전환은 사이토크롬 c (cyt c) 및 Apoptosis 유도 인자 (AIF)와 같은 전세포자멸 매개체의 전위를 촉진하며, 이들 모두 Apoptosis를 자극합니다. 결과적으로 이는 암세포가 Apoptosis에 의해 자살하도록 유도합니다.
|
| 생체 내(In vivo) |
Sodium Dichloroacetate (DCA)는 시험관 내 및 생체 내에서 Apoptosis(프로그램된 세포 사멸)를 유발하지 않고 세포 증식 억제제로 작용할 수 있습니다. 심장, 폐, 신장 또는 골수 독성이 없는 안전한 약물로 밝혀졌습니다. 가장 심각한 일반적인 부작용은 가역적인 말초 신경병증입니다. 이 화합물은 결장암, 전립선암, 난소암, 신경모세포종, 폐 유암종, 자궁경부암, 자궁내막암, 담관암, 육종 및 T세포 림프종을 포함한 여러 유형의 암에서 항암 활성을 나타냅니다. 다른 항신생물 작용도 제안되었습니다. 여기에는 혈관 신생 차단, HIF1-α 발현 변화, pH 조절자 V-ATPase 및 MCT1의 변경, PUMA, GLUT1, Bcl2 및 p53과 같은 다른 세포 생존 조절자가 포함됩니다. 이는 유방암의 고전이성 생체 내 모델에서 쥐의 폐 전이 부담을 유의하게 줄일 수 있습니다. 생체 내에서 DCA-Na 치료는 C57BL/6 마우스에서 체중에 영향을 미치지 않고 종양 직경, 부피 및 무게를 감소시키면서 20%의 생존율을 유도하고 전이를 방지합니다.
|
참조 |
|
적용 분야
| 방법 | 바이오마커 | 이미지 | PMID |
|---|---|---|---|
| Western blot | pPDH E1α / PDH E1α |
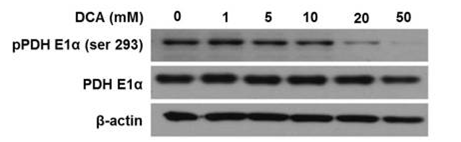
|
25630799 |
임상시험 정보
(데이터 출처 https://clinicaltrials.gov, 업데이트 날짜 2024-05-22)
| NCT 번호 | 모집 | 조건 | 스폰서/협력자 | 시작일 | 단계 |
|---|---|---|---|---|---|
| NCT06073106 | Not yet recruiting | Stroke|Traumatic Brain Injury|Knee Osteoarthritis|Breast Cancer |
Tan Tock Seng Hospital|Rehabilitation Research Institute of Singapore (RRIS)|Woodlands Health (WH) |
December 2023 | -- |
| NCT05810623 | Not yet recruiting | Upper Urinary Tract Urothelial Carcinoma|Bladder Cancer |
David D''Andrea|Medical University of Vienna |
June 1 2023 | Phase 3 |
| NCT05646485 | Recruiting | Bladder Cancer|Urothelial Carcinoma|Hematuria|Smoking Cessation |
University of Texas Southwestern Medical Center |
May 5 2023 | Not Applicable |
| NCT05460533 | Recruiting | B-cell Acute Lymphoblastic Leukemia |
Memorial Sloan Kettering Cancer Center|Novartis Pharmaceuticals |
July 12 2022 | Phase 2 |
