연구용
RRx-001 Dehydrogenase 억제제
제품 번호S8405
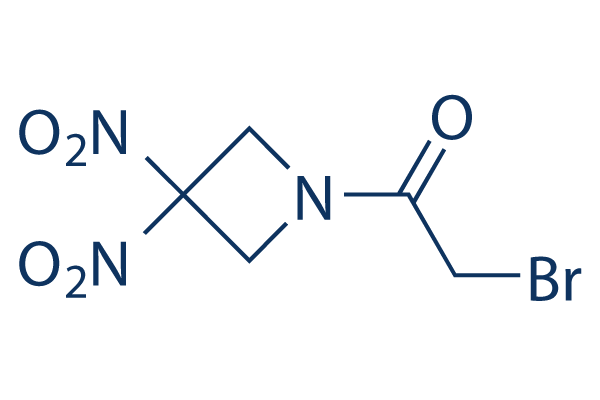
화학 구조
분자량: 268.02
품질 관리
화학 정보, 보관 및 안정성
| 분자량 | 268.02 | 화학식 | C5H6BrN3O5 |
보관 (수령일로부터) | |
|---|---|---|---|---|---|
| CAS 번호 | 925206-65-1 | SDF 다운로드 | 원액 보관 |
|
|
| 동의어 | N/A | Smiles | C1C(CN1C(=O)CBr)([N+](=O)[O-])[N+](=O)[O-] | ||
용해도
|
In vitro |
DMSO
: 54 mg/mL
(201.47 mM)
Ethanol : 14 mg/mL Water : Insoluble |
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| Targets/IC50/Ki |
G6PD
Nrf2-ARE
|
|---|---|
| 시험관 내(In vitro) |
RRx-001은 주요 세포 환원제인 NADPH의 적절한 수준을 유지하는 역할을 하는 펜토스 인산 경로의 핵심 효소인 포도당 6 인산 탈수소효소(G6PD)와의 간섭을 통해 적어도 부분적으로 항증식 효과를 발휘합니다. 이 화합물은 Hep G2, CACO-2 및 HT-29라는 세 가지 다른 암세포주에서 포도당 및 G6PD 효소 활성에 영향을 미칩니다. 이는 농도 의존적으로 G6PD 억제를 유도하고 포도당 소비를 증가시켰습니다. 이 화학 물질은 ROS/RNS 생성을 통해 p53 및 PARP-1을 유도합니다. 이는 빠르게 증식하는 세포의 3가지 중요한 대사 요구 사항인 생체 에너지, 거대 분자 생합성 및 세포질 환원 항상성 조작과 적어도 부분적으로 간섭함으로써 항암 활성을 발휘합니다. 이 약물은 Nrf2의 핵 전위 및 종양 세포에서 그 하류 효소인 HO-1 및 NQO1의 발현 활성화를 중재합니다. 후성 유전적 변화 외에도, 이는 산화환원 신호 전달 및 Nrf2, p53, PARP 분열, HIF1 알파 및 G6PD 활성과 같은 다양한 신호 경로의 산화환원 유도 조절 장애를 포함한 다면 발현 메커니즘을 통해 작용합니다. 또한 이중 가닥 DNA 손상에 대한 반응으로 p53 및 p21 활성을 유발하고 암세포 에너지 및 대사를 조절 장애시킵니다. 이 화합물은 ROS/RNS 생성을 통해 Nrf2-ARE 신호 경로의 강력한 활성제입니다.
|
| 생체 내(In vivo) |
RRx-001은 주변 세포 및 α-SMA가 풍부한 혈관을 가진 종양에서 단기 혈류 재분배에 대한 가능성을 보여줍니다. 이 화합물 단일 요법은 용량 제한 독성 없이 잘 견딥니다. 이는 Nrf2의 핵 전위를 촉진할 뿐만 아니라 마우스의 SCC VII 종양에서 내인성 Nrf2 발현을 상향 조절합니다.
|
참조 |
|
임상시험 정보
(데이터 출처 https://clinicaltrials.gov, 업데이트 날짜 2024-05-22)
| NCT 번호 | 모집 | 조건 | 스폰서/협력자 | 시작일 | 단계 |
|---|---|---|---|---|---|
| NCT02096341 | Terminated | Malignant Solid Tumor|Lymphomas |
EpicentRx Inc. |
April 2014 | Phase 1 |
