연구용
T0070907 PPARγ 길항제
제품 번호S2871
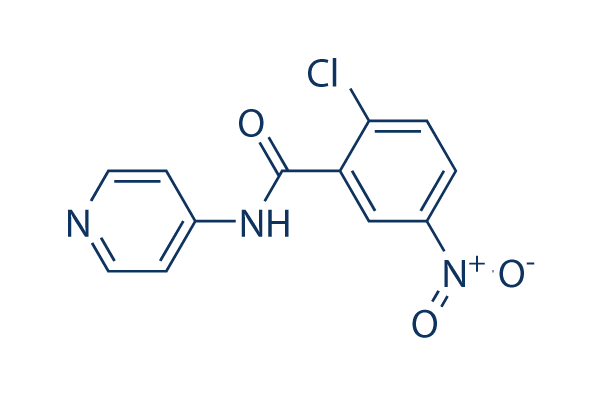
화학 구조
분자량: 277.66
품질 관리
세포 배양, 처리 및 작업 농도
| 세포주 | 분석 유형 | 농도 | 배양 시간 | 제형 | 활성 설명 | PMID |
|---|---|---|---|---|---|---|
| OR6 | Cytotoxicity assay | 72 hrs | Cytotoxicity against african green monkey OR6 cells after 72 hrs by WST1 assay, CC50=2.7μM. | 23891183 | ||
| OR6 | Antiviral assay | 72 hrs | Antiviral activity against HCV infected in african green monkey OR6 cells assessed as inhibition of viral RNA replication after 72 hrs by luciferase reporter gene assay, ED50=4.9μM. | 23891183 | ||
| 클릭하여 더 많은 세포주 실험 데이터 보기 | ||||||
화학 정보, 보관 및 안정성
| 분자량 | 277.66 | 화학식 | C12H8ClN3O3 |
보관 (수령일로부터) | |
|---|---|---|---|---|---|
| CAS 번호 | 313516-66-4 | SDF 다운로드 | 원액 보관 |
|
|
| 동의어 | N/A | Smiles | C1=CC(=C(C=C1[N+](=O)[O-])C(=O)NC2=CC=NC=C2)Cl | ||
용해도
|
In vitro |
DMSO
: 55 mg/mL
(198.08 mM)
Water : Insoluble Ethanol : Insoluble |
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| Targets/IC50/Ki |
PPARγ
|
|---|---|
| 시험관 내(In vitro) |
T0070907은 강력하고 선택적인 PPARγ 길항제입니다. 1 nM의 겉보기 결합 친화도로, 이 화합물은 인간 PPARγ2의 헬릭스 3에 있는 시스테인 313에서 PPARγ를 공유 결합으로 변형시킵니다. 이는 세포 기반 리포터 유전자 및 지방세포 분화 분석 모두에서 PPARγ 기능을 차단합니다. PPARγ 길항제로서의 역할과 일관되게, 이 화학물질은 균일한 시간 분해 형광 기반 분석에서 보조활성인자 유래 펩타이드의 작용제 유도 PPARγ 모집을 차단하고 글루타티온 S-트랜스퍼라제 풀다운 분석 및 PPARγ/레티노이드 X 수용체 (RXR) α 의존적 젤 시프트 분석 모두에서 전사적 보조억제인자 NCoR의 PPARγ 모집을 촉진합니다. 돌연변이 수용체 연구는 PPARγ 리간드 결합 도메인의 헬릭스 12의 형태에 영향을 미침으로써 이러한 보조인자 단백질과의 PPARγ 상호작용을 조절함을 시사합니다. 흥미롭게도, T0070907 유도 NCoR의 PPARγ/RXRα 이종이합체로의 모집은 RXRα 작용제 LGD1069와의 동시 처리로 거의 완전히 역전될 수 있는 반면, 이 화합물 처리는 LGD1069 유도 보조활성인자의 PPARγ/RXRα 이종이합체로의 모집에 미미한 영향만 미칩니다. 이 화학 처리제는 증식, 침습 및 이동을 억제하지만 세포자멸사에는 유의미한 영향을 미치지 않습니다. 우성 음성 (Δ462) 수용체를 이용한 분자적 억제는 유사한 결과를 산출합니다. 또한 PPARγ의 인산화 및 DNA 결합 능력의 용량 의존적 감소를 매개하며, 미토겐 활성화 단백질 키나제 신호 전달에 직접적인 영향을 미칠 수 있습니다. |
| 키나아제 분석 |
리간드 결합 분석
|
|
T0070907의 PPAR에 대한 결합 친화도를 결정하기 위해 다음과 같은 수정 사항과 함께 섬광 근접 분석(SPA)이 수행됩니다. 90μl 반응액에는 SPA 버퍼(10 mM KH2PO4, 10 mM KH2PO4, 2 mM EDTA, 50 mM NaCl, 1 mM 디티오트레이톨, 2 mM CHAPS, 10% (v/v) 글리세롤, pH 7.1), 50 ng의 GST-PPARγ(또는 150 ng의 GST-PPARα, GST-PPARδ), 5 nM 3H 표지된 방사성 리간드 및 Me2SO에 있는 이 화합물 5 μl가 포함됩니다. 실온에서 1시간 배양 후, 폴리리신 코팅된 SPA 비드 10 μl(SPA 버퍼에 20 mg/ml)를 첨가하고, 혼합물을 Packard Topcount에서 판독하기 전에 1시간 동안 배양합니다.
|
|
| 생체 내(In vivo) |
지질다당류 전처리는 심각한 내독소혈증으로 인한 신장 기능 장애, 간세포 손상 및 순환 부전의 발생과 인터루킨-1 [베타]의 혈장 수준 증가를 유의하게 완화합니다. 이 화합물은 지질다당류 전처리로 얻어지는 이러한 모든 유익한 효과를 완화할 수 있습니다 |
참조 |
|
