연구용
Cilomilast PDE 억제제
제품 번호S1455
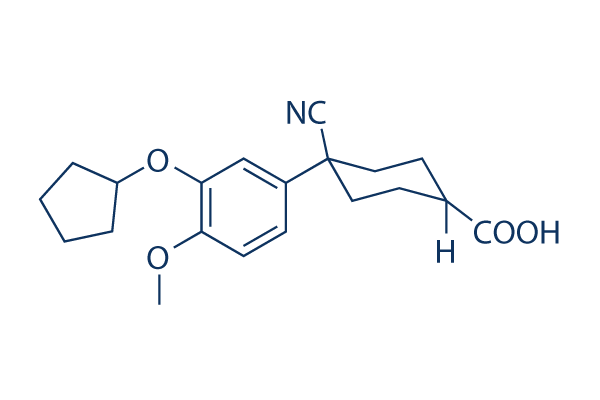
화학 구조
분자량: 343.42
품질 관리
세포 배양, 처리 및 작업 농도
| 세포주 | 분석 유형 | 농도 | 배양 시간 | 제형 | 활성 설명 | PMID |
|---|---|---|---|---|---|---|
| Sf9 cells | Function assay | Inhibition of human Phosphodiesterase 4A isoform using construct representing the common region of spliced variants expressed as GST-fusion proteins in Sf9 cells, IC50=0.038 μM | ||||
| sf21 cells | Function assay | Inhibition of human full length PDE4A4 expressed in baculovirus infected sf21 cells, IC50=0.062 μM | ||||
| human peripheral blood mononuclear cells | Function assay | Inhibition of TNF-alpha release from human peripheral blood mononuclear cells, IC50=3.467 μM | ||||
| U937 cells | Function assay | Arbitary maximal response for cAMP elevation from baseline level was evaluated in Human U-937 cells, EC50=3.63 μM | ||||
| 클릭하여 더 많은 세포주 실험 데이터 보기 | ||||||
화학 정보, 보관 및 안정성
| 분자량 | 343.42 | 화학식 | C20H25NO4 |
보관 (수령일로부터) | |
|---|---|---|---|---|---|
| CAS 번호 | 153259-65-5 | SDF 다운로드 | 원액 보관 |
|
|
| 동의어 | SB-207499 | Smiles | COC1=C(C=C(C=C1)C2(CCC(CC2)C(=O)O)C#N)OC3CCCC3 | ||
용해도
|
In vitro |
DMSO
: 69 mg/mL
(200.92 mM)
Ethanol : 50 mg/mL Water : Insoluble |
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| 특징 |
Cilomilast has been used to treat chronic obstructive pulmonary disease (COPD) for many years.
|
|---|---|
| Targets/IC50/Ki |
LPDE4
(Cell-free assay) 100 nM
HPDE4
(Cell-free assay) 120 nM
|
| 시험관 내(In vitro) |
Cilomilast는 U937 세포에서 cAMP 함량의 농도 의존적 증가를 유도합니다. 이 화합물은 U937 세포에서 cAMP 함량의 농도 의존적 증가를 유도합니다. 분리된 인간 단핵구에서, 이 화합물과 (R)-rolipram은 LPS 유발 TNF-α 형성 억제에 대해 각각 -log (IC50) 7.0과 7.2로 동등한 효능을 보입니다. 이 화합물과 (R)-rolipram 둘 다 fMLP 유발 인간 호중구 탈과립을 완만하게 예방합니다. 이 화합물과 (R)-rolipram은 호중구 활성 억제에 대해 각각 -log (IC50) 7.1과 6.4로 동등한 효능을 보입니다. 이 화학물질은 대조군과 비교하여 각막의 TNF-α 및 결막의 IL-1α, IL-1β, TNF-α 발현을 유의하게 감소시킵니다. 이 치료는 중심 및 주변 각막에서 CD11b+ 항원 제시 세포의 존재를 현저히 감소시키고, 결막에서 IL-6, IL-23, IL-17 사이토카인의 발현 감소로 이어집니다. 더욱이, 배액 림프절에서 IL-17 및 IL-23의 발현을 감소시킵니다. 이 화합물은 TLR4 발현, IL-8 방출 및 호중구 화학주성 활성을 감소시키며, IP-10 방출 및 림프구 화학주성 활성을 증가시킵니다.
|
| 생체 내(In vivo) |
Cilomilast는 4.9 mg/kg의 경구 ED50으로 인간 TNFα 생산을 억제합니다. TNFα 생산에 대한 동등한 효능과는 대조적으로, 이 화합물 (ED50 = 2.3 mg/kg, p.o.)은 항우울제 활성 모델인 레세르핀 유발 저체온증을 역전시키는 데 R-rolipram (ED50 = 0.23 mg/kg, p.o.)보다 10배 덜 강력합니다. 시간 경과 연구에서 이 화학물질 (30 mg/kg, p.o.)은 최소 10시간 동안 TNFα 생산을 억제합니다. Balb/c 마우스에서 만성 옥사졸론 유발 접촉 과민성 모델에서 생체 내 인터루킨-4 생산을 조절하는 이 화합물의 능력이 평가되었습니다. 이 화학물질 (1000 μg)의 국소 투여는 병변 내 인터루킨-4 농도를 억제합니다. 경구 투여된 Cilomilast는 난백 알레르기 유발 Brown Norway 랫트의 기도에서 기관지폐포 세척액 내 인터루킨-4, TNF-α, 시스테인 류코트리엔 생산뿐만 아니라 백혈구 침윤을 용량 의존적으로 억제합니다 .
|
참조 |
|
