연구용
Cidofovir DNA/RNA Synthesis 억제제
제품 번호S1516
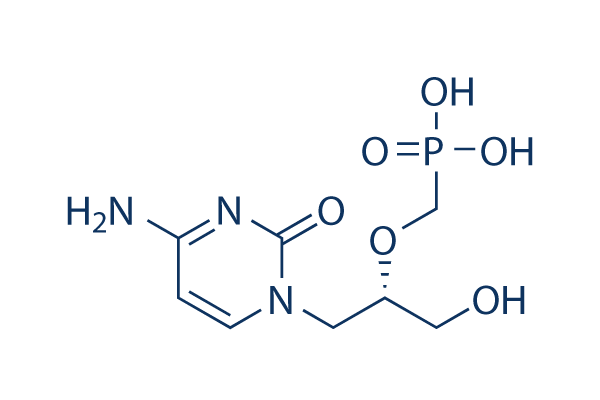
화학 구조
분자량: 279.19
품질 관리
| 관련 타겟 | HDAC PARP ATM/ATR DNA-PK WRN Topoisomerase PPAR Sirtuin Casein Kinase eIF |
|---|---|
| 기타 DNA/RNA Synthesis 억제제 | CX-5461 (Pidnarulex) B02 SCR7 Favipiravir (T-705) EED226 RK-33 BMH-21 Triapine (3-AP) Carmofur YK-4-279 |
세포 배양, 처리 및 작업 농도
| 세포주 | 분석 유형 | 농도 | 배양 시간 | 제형 | 활성 설명 | PMID |
|---|---|---|---|---|---|---|
| HEL cells | Function assay | Compound was tested for anti-viral activity against HSV-1(KOS) in HEL cells, EC50=0.57 μM | ||||
| MRC-5 cells | Function assay | Inhibitory activity against cytopathic effect of HSV-2(E 194) in MRC-5 cells, IC50=10 μM | ||||
| NHDF cells | Function assay | Inhibitory activity against replication of HCMV in NHDF cells, IC50=0.5 μM | ||||
| HFF cells | Function assay | Antiviral activity against Vaccinia virus Copenhagen in HFF cells assessed as reduction in cytopathogenicity, EC50=3.2 μM | ||||
| HFF cells | Function assay | Antiviral activity against Cowpox virus Brighton in HFF cells assessed as reduction in cytopathogenicity, EC50=7.1 μM | ||||
| HFF cells | Function assay | Antiviral activity against vaccinia virus Copenhagen measured as cytopathogenicity in HFF cells, EC50=6.9 μM | ||||
| bone marrow cells | Cytotoxicity assay | Cytotoxicity against human bone marrow cells assessed as inhibition of colony forming unit of granulocyte/macrophage, IC50=10 μM | ||||
| HFF cells | Function assay | Antiviral activity against Human CMV T2241 in HFF cells by SEAP assay, IC50=0.3 μM | ||||
| MRC5 cells | Function assay | Antiviral activity against Human CMV Towne in MRC5 cells by PRA, IC50=0.3 μM | ||||
| UC1B cells | Function assay | Antiviral activity against Murine polyomavirus MN/RDE Toronto in mouse UC1B cells assessed as reduction of virus-induced cytopathogenicity, EC50=13 μM | ||||
| african green monkey Vero cells | Function assay | Antiviral activity against Herpes simplex virus 1 F infected in african green monkey Vero cells assessed as plaque reduction after 36 to 48 hrs, EC50=14.4 μM | ||||
| HEL cells | Function assay | 3 days | Antiviral activity against HCMV AD169 infected in HEL cells assessed as reduction of virus-induced cytopathogenicity after 3 days, EC50=0.41 μM | |||
| HEL cells | Function assay | 3 days | Antiviral activity against HCMV Davis infected in HEL cells assessed as reduction of virus-induced cytopathogenicity after 3 days, EC50=0.41 μM | |||
| HFF cells | Function assay | Antiviral activity against Cytomegalovirus CMV T2211 infected in HFF cells by SEAP reporter gene assay, EC50=0.22 μM | ||||
| HEL cells | Function assay | Antiviral activity against ganciclovir-resistant HCMV AD169 clone 4 infected in HEL cells assessed as inhibition of virus-induced cytopathicity, EC50=0.74 μM | ||||
| HEL cells | Function assay | Antiviral activity against HCMV Davis infected in human HEL cells assessed inhibition of virus-induced cytopathicity after 7 days postinfection, EC50=0.5 μM | ||||
| HEL cells | Function assay | Antiviral activity against HCMV AD169 infected in human HEL cells assessed inhibition of virus-induced cytopathicity after 7 days postinfection, EC50=0.3 μM | ||||
| HEL cells | Function assay | Antiviral activity against foscarnet-resistant HCMV AD169 clone C infected in HEL cells assessed as inhibition of virus-induced cytopathicity, IC50=0.045 μM | ||||
| HFF | Proliferation assay | 3 days | Antiproliferative activity against HFF after 3 days by coulter counter assay, EC50=1.9 μM | |||
| HeLaS3 cells | Function assay | 3-5 days | Antiviral activity against Vaccinia virus IHD-J ATCC VR-156 infected in HeLaS3 cells after 3 to 5 days by plaque assay, EC50=18.74 μM | |||
| HSB2 cells | Function assay | 7 days | Antiviral activity against Human herpesvirus 6 GS infected in human HSB2 cells assessed as decrease in viral DNA accumulation after 7 days, EC50=2.7 μM | |||
| A549 cells | Function assay | Antiviral activity against Human adenovirus type 11p slobitski infected in A549 cells assessed as inhibition of DNA replication by QPCR assay, EC50=16.5 μM | ||||
| HFF cells | Function assay | Antiviral activity against Cowpox virus (Brighton Red) infected in human HFF cells assessed as reduction in viral-induced cytopathic effect by neutral red uptake assay, EC50=6.7 μM | ||||
| 클릭하여 더 많은 세포주 실험 데이터 보기 | ||||||
화학 정보, 보관 및 안정성
| 분자량 | 279.19 | 화학식 | C8H14N3O6P |
보관 (수령일로부터) | |
|---|---|---|---|---|---|
| CAS 번호 | 113852-37-2 | SDF 다운로드 | 원액 보관 |
|
|
| 동의어 | HPMPC, GS 0504 | Smiles | C1=CN(C(=O)N=C1N)CC(CO)OCP(=O)(O)O | ||
용해도
|
In vitro |
Water : 3 mg/mL
DMSO
: Insoluble
Ethanol : Insoluble |
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| 시험관 내(In vitro) |
Cidofovir는 배양된 세포에서 인간 거대세포바이러스(HCMV) 감염을 억제합니다. 이 화합물은 감염 48시간 후 세포에 첨가되었을 때에도 CMV 플라크 형성을 억제하며, Davis 균주에 대해 0.9 μg/mL, AD-169 균주에 대해 1.6 μg/mL의 IC50을 보였습니다. 또한 헤르페스 심플렉스 바이러스 감염도 억제합니다. 뿐만 아니라, 이 화학물질은 원숭이 신장 세포에서 HSV-1에 의해 유도된 세포 융합을 차단하고 HSV-1 특이 단백질의 발현과 바이러스 DNA 합성을 차단합니다. |
|---|---|
| 생체 내(In vivo) |
Cidofovir (5 mg/kg/day)를 5일 동안 피하 투여하면 감염된 기니피그의 혈액, 비장, 폐 및 침샘에서 평균 바이러스 감염 역가가 유의하게 감소합니다. 이 화합물은 감염된 동물의 림프구 증가증과 비장의 평균 조직 지수를 유의하게 감소시킵니다. . HSV-1 또는 HSV-2에 피내 감염된 무모 쥐의 모든 증상(피부 병변, 뒷다리 마비, 사망률)을 억제합니다. 이 화합물의 가장 주목할 만한 특징은 감염 후 4일이 지나서도 단 한 번의 투여로 HSV-1 또는 HSV-2 감염에 대한 상당한 보호를 제공한다는 것입니다. 이 화학물질은 C57Bl6/J 마우스에 피하 이식된 마우스 흑색종 B16 세포에서 발생하는 고도로 공격적인 흑색종 종양의 성장을 억제합니다. |
참조 |
|
임상시험 정보
(데이터 출처 https://clinicaltrials.gov, 업데이트 날짜 2024-05-22)
| NCT 번호 | 모집 | 조건 | 스폰서/협력자 | 시작일 | 단계 |
|---|---|---|---|---|---|
| NCT04542252 | Completed | Drug Drug Interaction |
SymBio Pharmaceuticals |
November 9 2020 | Phase 1 |
| NCT01610765 | Withdrawn | Herpes Simplex Virus |
University of Alabama at Birmingham |
January 2016 | Phase 1|Phase 2 |
| NCT01816646 | Completed | Blood And Marrow Transplantation |
M.D. Anderson Cancer Center|Gilead Sciences |
September 2013 | Phase 1 |
| NCT00780182 | Completed | Healthy |
Chimerix|National Institutes of Health (NIH) |
October 2008 | Phase 1 |
