연구용
Crizotinib hydrochloride c-Met 억제제
제품 번호S5190
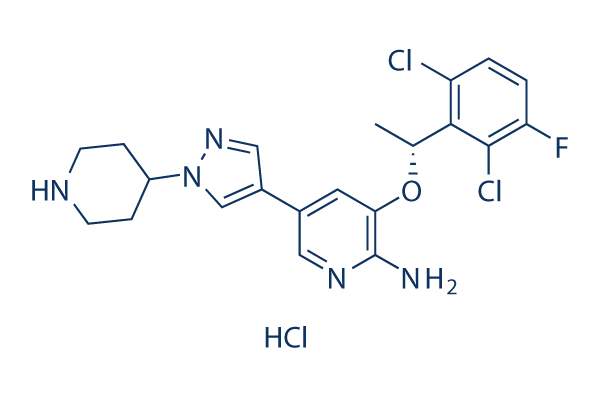
화학 구조
분자량: 486.8
품질 관리
| 관련 타겟 | EGFR VEGFR PDGFR FGFR Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| 기타 c-Met 억제제 | Tepotinib Dihexa SGX-523 PHA-665752 Foretinib SU11274 BMS-777607 JNJ-38877605 Tivantinib PF-04217903 |
화학 정보, 보관 및 안정성
| 분자량 | 486.8 | 화학식 | C21H23Cl3FN5O |
보관 (수령일로부터) | 3 years -20°C powder |
|---|---|---|---|---|---|
| CAS 번호 | 1415560-69-8 | -- | 원액 보관 |
|
|
| 동의어 | Xalkori, PF-02341066 hydrochloride | Smiles | Cl.CC(OC1=C(N)N=CC(=C1)C2=C[N](N=C2)C3CCNCC3)C4=C(Cl)C=CC(=C4Cl)F | ||
용해도
|
In vitro |
DMSO
: 97 mg/mL
(199.26 mM)
Water : 97 mg/mL Ethanol : 97 mg/mL |
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| Targets/IC50/Ki |
ROS1
(Cell-free assay) <0.025 nM(Ki)
c-Met
(Cell-based assay) 11 nM
NPM-ALK
(Cell-based assay) 24 nM
|
|---|---|
| 시험관 내(In vitro) |
PF-2341066은 mIMCD3 마우스 또는 MDCK 개 상피세포에서 c-Met 인산화에 대해 각각 5 nM 및 20 nM의 IC50으로 유사한 효능을 나타냅니다. PF-2341066은 c-Met ATP-결합 부위 돌연변이 V1092I 또는 H1094R 또는 P-루프 돌연변이 M1250T를 발현하도록 조작된 NIH3T3 세포에 대해 각각 19 nM, 2 nM 및 15 nM의 IC50으로 야생형 수용체를 발현하는 NIH3T3 세포의 IC50인 13 nM과 비교하여 개선되거나 유사한 활성을 보입니다. 대조적으로, c-Met 활성화 루프 돌연변이 Y1230C 및 Y1235D를 발현하도록 조작된 세포에 대해 PF-2341066의 효능에 현저한 변화가 관찰되며, 야생형 수용체와 비교하여 각각 127 nM 및 92 nM의 IC50을 보였습니다. PF-2341066은 또한 NCI-H69 및 HOP92 세포에서 c-Met의 인산화를 강력하게 방지하며, 각각 13 nM 및 16 nM의 IC50을 보였고, 이들 세포는 내인성 c-Met 변이체 R988C 및 T1010I를 각각 발현합니다. PF-2341066은 VEGFR2 및 PDGFRβ RTK에 대해 >1,000배, IRK 및 Lck에 대해 >250배, Tie2, TrkA 및 TrkB에 대해 ~40~60배 선택적이며, 모두 c-Met과 비교한 것입니다. PF-2341066은 RON 및 Axl RTK에 대해 20~30배 선택적입니다. 대조적으로, PF-2341066은 KARPAS299 인간 역형성 대세포 림프종(ALCL) 세포주에 의해 발현되는 ALK RTK의 뉴클레오포스민(NPM)-anaplastic lymphoma kinase (ALK) 발암성 융합 변이체에 대해 거의 동등한 24 nM의 IC50을 보입니다. PF-2341066은 암세포의 c-Met 의존성 신생물 표현형과 내피세포의 혈관신생 표현형을 억제합니다. PF-2341066은 인간 GTL-16 위암 세포 성장을 9.7 nM의 IC50으로 억제합니다. PF-2341066은 GTL-16 세포에서 8.4 nM의 IC50으로 세포자멸사를 유도합니다. PF-2341066은 HGF-자극된 인간 NCI-H441 폐암 세포 이동 및 침윤을 각각 11 nM 및 6.1 nM의 IC50으로 억제합니다. PF-2341066은 MDCK 세포 산란을 16 nM의 IC50으로 억제합니다. PF-2341066은 HGF-자극된 c-Met 인산화, 세포 생존 및 Matrigel 침윤을 각각 11 nM, 14 nM 및 35 nM의 IC50으로 방지합니다. 또한, PF-2341066은 혈청-자극된 HMVEC 분지형 관형성(혈관 형성)을 피브린 겔에서 방지합니다. |
| 키나아제 분석 |
세포 키나아제 인산화 ELISA 분석
|
|
세포는 10% 소 태아 혈청(FBS)이 보충된 배지에 96웰 플레이트에 시드되고 24시간 후 혈청 없는 배지 [0.04% 소 혈청 알부민(BSA) 함유]로 옮겨집니다. 리간드 의존성 RTK 인산화를 조사하는 실험에서는 해당 성장 인자가 최대 20분 동안 첨가됩니다. PF-2341066으로 세포를 1시간 동안 및/또는 지정된 시간 동안 적절한 리간드로 세포를 배양한 후, 세포는 1mM Na3VO4가 보충된 HBSS로 한 번 세척되고 세포에서 단백질 용해물이 생성됩니다. 이어서, 선택된 Protein Tyrosine Kinase의 인산화는 96웰 플레이트를 코팅하는 데 사용되는 특정 포획 항체와 인산화된 티로신 잔기에 특이적인 검출 항체를 사용하는 샌드위치 ELISA 방법으로 평가됩니다. 항체 코팅된 플레이트는 (a) 4°C에서 밤새 단백질 용해물 존재하에 배양되고; (b) 1% Tween 20이 포함된 PBS로 7회 세척되고; (c) 서양 고추냉이 과산화효소-접합된 항-총-인산화 티로신 (PY-20) 항체 (1:500)에 30분 동안 배양되고; (d) 다시 7회 세척되고; (e) 0.09 N H2SO4를 첨가하여 중단되는 비색 반응을 시작하기 위해 3,3′,5,5′-테트라메틸 벤지딘 과산화효소 기질에 배양되고; (f) 분광광도계를 사용하여 450 nm에서 흡광도를 측정합니다.
|
|
| 생체 내(In vivo) |
GTL-16 모델에서 PF-2341066은 50 mg/kg/일 및 75 mg/kg/일 치료 코호트 모두에서 43일 투여 일정 동안 평균 종양 부피가 60% 감소하면서 대규모로 확립된 종양(>600 mm3)의 현저한 퇴행을 유발하는 능력을 보여줍니다. 또 다른 연구에서 PF-2341066은 50 mg/kg/일에서 3개월 치료 일정 동안 12마리 중 1마리만이 종양 성장률의 유의미한 증가를 보이며 GTL-16 종양 성장을 3개월 이상 완전히 억제하는 능력을 보여줍니다. NCI-H441 NSCLC 모델에서 38일 PF-2341066 투여 주기 동안 50 mg/kg/일에서 평균 종양 부피가 43% 감소하는 것이 관찰됩니다. Caki-1 RCC 모델에서 33일 PF-2341066 투여 주기 동안 50 mg/kg/일에서 각 종양의 부피가 최소 30% 감소하는 것과 관련된 평균 종양 부피의 53% 감소가 관찰됩니다. PF-2341066은 또한 U87MG 교모세포종 또는 PC-3 전립선암 이종이식 모델에서 50 mg/kg/일에서 확립된 종양 성장을 거의 완전히 방지하며, 연구 마지막 날 각각 97% 또는 84% 억제를 보입니다. 대조적으로, 50 mg/kg/일로 경구 투여된 PF-2341066은 MDA-MB-231 유방암 모델 또는 DLD-1 결장암 모델에서 종양 성장을 유의미하게 억제하지 않습니다. GTL-16 종양에서 12.5 mg/kg/일, 25 mg/kg/일 및 50 mg/kg/일에서 CD31 양성 내피세포의 유의미한 용량 의존적 감소가 관찰되며, 이는 MVD 억제가 항종양 효능과 용량 의존적 상관 관계를 보임을 나타냅니다. PF-2341066은 GTL-16 및 U87MG 모델 모두에서 인간 VEGFA 및 IL-8 혈장 수준의 유의미한 용량 의존적 감소를 보여줍니다. PF-2341066 경구 투여 후 GTL-16 종양에서 인산화된 c-Met, Akt, Erk, PLCλ1 및 STAT5 수준의 현저한 억제가 관찰됩니다.
|
참조 |
|
임상시험 정보
(데이터 출처 https://clinicaltrials.gov, 업데이트 날짜 2024-05-22)
| NCT 번호 | 모집 | 조건 | 스폰서/협력자 | 시작일 | 단계 |
|---|---|---|---|---|---|
| NCT06062810 | Not yet recruiting | Non-Small Cell Lung Cancer |
Han Xu M.D. Ph.D. FAPCR Sponsor-Investigator IRB Chair|Medicine Invention Design Inc |
March 28 2024 | Phase 2|Phase 3 |
| NCT04148066 | Completed | Carcinoma Non-Small-Cell Lung |
The Netherlands Cancer Institute|Roche Pharma AG |
July 17 2019 | Not Applicable |
| NCT03947385 | Recruiting | Metastatic Uveal Melanoma|Cutaneous Melanoma|Colorectal Cancer|Other Solid Tumors |
IDEAYA Biosciences |
June 28 2019 | Phase 1|Phase 2 |
| NCT03672643 | Terminated | ALK or ROS1-positive NSCLC |
Pfizer |
January 28 2019 | Phase 4 |
| NCT03439215 | Unknown status | Carcinoma Non-Small-Cell Lung |
Fondazione Ricerca Traslazionale|Clinical research technology Srl |
June 13 2017 | Phase 2 |
