연구용
Golvatinib (E7050) c-Met 억제제
제품 번호S2859
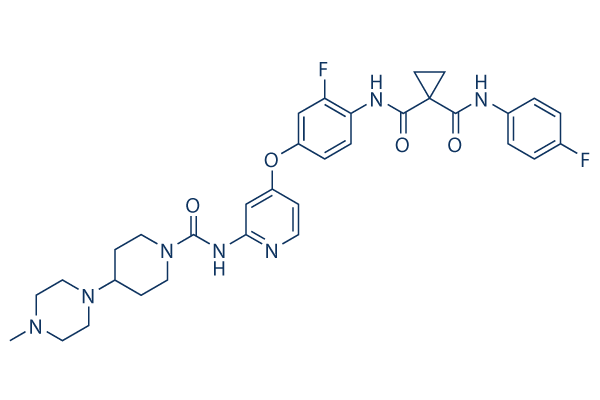
화학 구조
분자량: 633.69
품질 관리
| 관련 타겟 | EGFR VEGFR PDGFR FGFR Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| 기타 c-Met 억제제 | Tepotinib Dihexa SGX-523 PHA-665752 Foretinib SU11274 BMS-777607 JNJ-38877605 Tivantinib PF-04217903 |
화학 정보, 보관 및 안정성
| 분자량 | 633.69 | 화학식 | C33H37F2N7O4 |
보관 (수령일로부터) | |
|---|---|---|---|---|---|
| CAS 번호 | 928037-13-2 | SDF 다운로드 | 원액 보관 |
|
|
| 동의어 | N/A | Smiles | CN1CCN(CC1)C2CCN(CC2)C(=O)NC3=NC=CC(=C3)OC4=CC(=C(C=C4)NC(=O)C5(CC5)C(=O)NC6=CC=C(C=C6)F)F | ||
용해도
|
In vitro |
DMSO
: 20 mg/mL
(31.56 mM)
Water : Insoluble Ethanol : Insoluble |
몰농도 계산기
|
In vivo |
|||||
생체 내 제형 계산기 (투명한 용액)
1단계: 아래 정보 입력 (권장: 실험 중 손실을 고려하여 추가 동물 포함)
2단계: 생체 내 제형 입력 (이것은 계산기일 뿐 제형이 아닙니다. 용해도 섹션에 생체 내 제형이 없는 경우 먼저 당사에 문의하십시오.)
계산 결과:
작업 농도: mg/ml;
DMSO 원액 준비 방법: mg 약물 사전 용해 μL DMSO ( 원액 농도 mg/mL, 농도가 해당 약물 배치의 DMSO 용해도를 초과하는 경우 먼저 당사에 문의하십시오. )
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가μL PEG300, 혼합하고 투명하게 한 다음 추가μL Tween 80, 혼합하고 투명하게 한 다음 추가 μL ddH2O, 혼합하고 투명하게 합니다.
생체 내 제형 준비 방법: 취하다 μL DMSO 원액, 다음 추가 μL 옥수수 기름, 혼합하고 투명하게 합니다.
참고: 1. 다음 용매를 추가하기 전에 액체가 투명한지 확인하십시오.
2. 용매를 순서대로 추가해야 합니다. 다음 용매를 추가하기 전에 이전 추가에서 얻은 용액이 투명한 용액인지 확인해야 합니다. 와동, 초음파 또는 뜨거운 물 중탕과 같은 물리적 방법을 사용하여 용해를 도울 수 있습니다.
작용 메커니즘
| Targets/IC50/Ki |
c-Met
14 nM
VEGFR2
16 nM
|
|---|---|
| 시험관 내(In vitro) |
시험관 내 연구에 따르면 Golvatinib (E7050)은 c-Met 및 VEGFR-2의 인산화를 강력하게 억제합니다. 또한 HGF 또는 VEGF로 자극된 c-Met 증폭 종양 세포 및 내피 세포의 성장을 강력하게 억제합니다. 이 화합물은 시험관 내에서 Met/Gab1/PI3K/Akt 경로를 차단함으로써 EGFR 돌연변이 폐암 세포주에서 외인성 및/또는 내인성 HGF에 의해 유도되는 모든 가역적, 비가역적 및 돌연변이 선택적 EGFR-TKI에 대한 저항성을 회피합니다. 또한 HGF에 지속적으로 노출되어 유도되는 게피티니브 저항성 HCC827 세포의 출현을 방지합니다.
|
| 키나아제 분석 |
웨스턴 블롯 분석
|
|
c-Met 및 VEGFR-2의 인산화 상태는 웨스턴 블롯 분석으로 검출됩니다. c-Met의 경우, MKN45 세포를 37 °C에서 2시간 동안 완전 배지에 Golvatinib (E7050)의 연속 희석액과 함께 배양합니다. VEGFR-2의 경우, HUVEC는 0.5% FBS를 포함하는 인간 내피 혈청-프리 배지에서 24시간 동안 굶깁니다. 그 후 HUVEC는 이 화합물의 연속 희석액과 함께 1시간 동안 배양한 다음, 20 ng/mL의 인간 VEGF와 함께 5분 동안 배양합니다. 세포는 용해 버퍼(50 mM HEPES [pH 7.4], 150 mM NaCl, 10% 글리세롤, 1% Triton X-100, 1.5 mM MgCl2, 1 mM EDTA [pH 8.0], 100 mM NaF, 1 mM 페닐메틸설포닐 플루오라이드, 1 mM 오르토바나데이트 나트륨, 10 μg/mL 아프로티닌, 50 μg/mL 류펩틴, 1 μg/mL 펩스타틴 A)로 용해됩니다. 절제된 종양 샘플은 25 mM β-글리세로포스페이트 및 0.5% (v/v) 인산화효소 억제제 칵테일 2를 포함하는 용해 버퍼로 4 °C에서 균질화됩니다. 세포 잔해는 4 °C에서 20분 동안 17 860g으로 원심분리하여 제거됩니다. 5-20 μg의 단백질을 포함하는 상층액의 분취액은 환원 조건에서 SDS-PAGE를 수행합니다. 단백질은 PVDF 멤브레인으로 전사된 다음, 0.05% Tween-20과 5% 탈지유 또는 5% BSA를 포함하는 TBS로 블로킹됩니다. 멤브레인은 다음 항체로 조사됩니다: 항-c-Met 다클론 항체 (C-28) 및 항-VEGFR-2 다클론 항체 (C-20); 마우스 항-포스포티로신 클론 4G10; 및 항-VEGFR-2 다클론 항체, 항-포스포-VEGFR-2 (Tyr996) 다클론 항체, 및 항-포스포-c-Met (Tyr1234/1235) 다클론 항체. 검출은 Super Signal 강화 화학발광 키트를 사용하여 수행됩니다. 면역 반응성 밴드는 Image Master-VDS-CL 검출 시스템으로 화학발광을 통해 시각화됩니다. 각 밴드의 강도는 이미지 분석기를 사용하여 측정됩니다.
|
|
| 생체 내(In vivo) |
Golvatinib (E7050)은 생체 내에서 종양의 c-Met 및 VEGFR-2 인산화 억제를 보여주며, 이종이식 모델에서 종양 성장 및 혈관신생을 강력하게 억제합니다. c-Met 증폭을 포함하는 일부 종양 계통을 이 화합물의 고용량(50–200 mg/kg)으로 치료하면 종양 퇴행 및 소멸이 유도됩니다. 복막 전이 모델에서는 복막 종양에 대한 항종양 효과뿐만 아니라 치료된 마우스의 수명도 유의하게 연장됨을 보여줍니다. 또 다른 이종이식 연구에서는 HGF-형질감염 Ma-1 (Ma-1/HGF) 세포에 의해 생성된 종양이 벡터 대조군 종양보다 더 혈관신생적이며 ZD1839에 대한 저항성을 보입니다. E7050 단독은 혈관신생을 억제하고 Ma-1/HGF 종양의 성장을 지연시키며, ZD1839와 병용할 경우 종양 성장의 현저한 퇴행을 유도합니다.
|
참조 |
|
임상시험 정보
(데이터 출처 https://clinicaltrials.gov, 업데이트 날짜 2024-05-22)
| NCT 번호 | 모집 | 조건 | 스폰서/협력자 | 시작일 | 단계 |
|---|---|---|---|---|---|
| NCT01355302 | Terminated | Advanced or Metastatic Solid Tumors|Previously Untreated Gastric Cancer |
Eisai Inc.|Quintiles Inc. |
November 2011 | Phase 1|Phase 2 |
| NCT01433991 | Terminated | Advanced Solid Tumors |
Eisai Inc. |
October 13 2011 | Phase 1|Phase 2 |
| NCT01332266 | Completed | Platinum-Resistant Squamous Cell Carcinoma of the Head and Neck |
Eisai Inc.|PharmaBio Development Inc. |
September 19 2011 | Phase 1|Phase 2 |
| NCT01271504 | Completed | Hepatocellular Carcinoma |
Eisai Inc.|PharmaBio Development Inc. |
July 19 2011 | Phase 1|Phase 2 |
| NCT02533102 | Completed | Healthy Subjects |
Eisai Limited|Eisai Inc. |
November 2010 | Phase 1 |
| NCT00921869 | Completed | Solid Tumors |
Eisai Co. Ltd.|Eisai Inc. |
October 2009 | Phase 1 |
